Résumés
Résumé
Les écosystèmes marins côtiers sont des milieux de plus en plus affectés par l’activité humaine à cause des rejets urbains et l’utilisation de l’océan comme dépotoir pouvant mener à de hauts niveaux de pollution. L’objectif de cette étude était de déterminer les profils de concentration en éléments traces métalliques (Cd, Cr, Cu, Co, Ni, Pb et Zn) des sédiments dans des zones présumées être contaminées par les rejets des eaux usées à Dakar et d’évaluer leur qualité. Pour ce faire, des échantillons de sédiments ont été prélevés au niveau de cinq points d’évacuation des eaux usées vers la mer à Dakar (Sénégal). Les résultats montrent des caractéristiques géochimiques (granulométrie, alcalinité, teneur en carbone organique et en soufre) comparables. L’évaluation de la qualité des sédiments a été effectuée par le calcul de divers indices. Un enrichissement important des sédiments en cadmium et en plomb a surtout été noté. L’Indice de Pollution Sédimentaire (IPS), qui estime le degré de contamination d’un site en fonction de la toxicité relative de chaque métal considéré, fait état d’une forte pollution, voire même d’une dangerosité des sédiments étudiés. En effet, le cadmium et le plomb, présents en fortes teneurs dans les sites, contribuent respectivement à l’ordre de 94 % et 5 % à la dangerosité potentielle des sédiments (selon le classement de l’indice de pollution sédimentaire) alors que le zinc, le cuivre, le nickel et le chrome, également présents en fortes concentrations, ne représentent que 1 % de la pollution globale. Des corrélations positives élevées et modérées sont observées entre Pb/Cd, Pb/Co, Cr/Cu, Cr/Zn, Cr/Fe, Cr/Mn, Cu/Ni, Cu/Fe, Cu/Mn et Zn/Mn, indiquant leurs sources communes possibles à partir des activités industrielles et/ou urbaines ainsi que des comportements comparables dans le sédiment.
Mots-clés :
- Métaux lourds,
- pollution sédimentaire,
- activités urbaines,
- eaux usées,
- Dakar
Abstract
Coastal marine environments are increasingly affected by human activity because of urban waste, and use of the ocean as a dumping ground could lead to high levels of pollution. The objective of this study was to determine the concentration profiles of trace metals (Cd, Cr, Cu, Co, Ni, Pb and Zn) in sediments in areas suspected to be contaminated by discharges of wastewater from Dakar, and to evaluate the quality of the sediments. To do this, sediment samples were collected at five points of sewage discharge into the sea near Dakar (Senegal). The results show comparable geochemical characteristics (size, alkalinity, organic carbon content and sulfur content) at the different sites. The assessment of sediment quality was performed by calculating various indices. A substantial enrichment of sediment cadmium and lead was especially noted. The Sediment Pollution Index (SPI), which estimates the degree of contamination of a site based on the relative toxicity of each metal in question, indicated a high degree of pollution or even an environmental hazard for the sediments studied. Indeed, cadmium and lead are present at high concentrations at the sites, each contributing about 94% and 5% to the potential hazard of the sediments (ranked by the SPI index), whereas zinc, copper, nickel and chromium, also present at high concentrations, contribute only about 1% to the overall pollution. High and moderate positive correlations are observed between Pb/Cd, Pb/Co, Cr/Cu, Cr/Zn, Cr/Fe, Cr/Mn, Cu/Ni, Cu/Fe, Cu/Mn and Zn/Mn, indicating their possible common origin from industrial and/or urban sources, and their comparable behavior in the sediment.
Keywords:
- Trace metals,
- Sediment pollution,
- Urban activities,
- Wastewaters,
- Dakar
Corps de l’article
1. Introduction
Les écosystèmes marins côtiers sont des milieux de plus en plus affectés par l’activité humaine. L’industrialisation et le développement urbain, agricole ou touristique des villes en zone côtière sont les principales causes de l’augmentation de la pression exercée sur ces milieux (DABY, 2006; HUANG et al., 2007; MEMET et BÜLENT, 2012; RAO et al., 2007; SULTAN et al., 2011; XUELU et CHEN-TUNG, 2012). Les industries métallurgiques et minières connues être des sources de contamination métallique de l’environnement sont généralement implantées dans des zones côtières (AHN et al., 2005; LEE et CORREA, 2005; ROYCHOUDHURY et STARKE, 2006). De plus, les rejets urbains et l’utilisation de l’océan comme dépotoir peuvent mener à de hauts niveaux de pollution dans les écosystèmes marins côtiers (D’ADAMO et al., 2008; RAO et al., 2007; SMOLDERS et al., 2003). En effet, les eaux usées qui, dans de nombreux pays, ne sont que peu ou pas traitées, transportent et déversent de nombreux polluants dans les eaux côtières favorisant ainsi la bioaccumulation d’éléments toxiques dans les organismes marins dont le transport le long de la chaîne alimentaire représente un danger pour la santé humaine (BOENING, 1999; DABY, 2006).
Au Sénégal, la région de Dakar, qui représente 0,3 % de la superficie du pays, concentre plus de 80 % des industries au plan national (OIS, 2010) et plus de 25 % de la population. Malgré cette pression humaine et industrielle, Dakar ne dispose que d’un réseau d’évacuation des eaux usées et pluviales de 623 km avec une seule station d’épuration et de traitement des eaux usées. Cette station, qui a un débit moyen journalier de 9 600 m3, ne traite que 13 % du volume d’eaux usées produit à Dakar (ONAS, 2005). De plus, 70 % des effluents collectés proviennent des industries (raffinerie, huilerie, poissonnerie, brasserie) (GAYE et NIANG, 2002). Dès lors, d'importantes quantités d'eaux usées domestiques et industrielles contenant divers polluants (métaux lourds, colorants, polluants organiques etc.) sont ainsi rejetées en permanence dans la mer, ce qui s'est traduit par une dégradation de la qualité du milieu aquatique.
Ce constat a suscité des interrogations quant à la teneur en éléments chimiques des eaux côtières de Dakar, en particulier en métaux lourds, si l’on sait que ces métaux ne sont pas biodégradables et peuvent entraîner des effets néfastes sur la flore aquatique, les ressources halieutiques et sur les êtres humains. Or, à notre connaissance, aucune étude sur la pollution métallique de l’eau et des sédiments n’a été effectuée pour diagnostiquer la qualité du milieu. L’objectif de cette étude est de déterminer les profils de concentration en éléments traces métalliques (Cd, Cr, Cu, Co, Ni, Pb et Zn) des sédiments dans des zones présumées être contaminées par les rejets des eaux usées à Dakar et d’évaluer leur qualité. En effet, les sédiments contaminés constituent des sources potentielles de pollution de la colonne d’eau suite à des perturbations physiques (dragage) ou biogéochimiques (BOUGHRIET et al., 2007).
2. Matériel et méthode
2.1 Échantillonnage et traitement
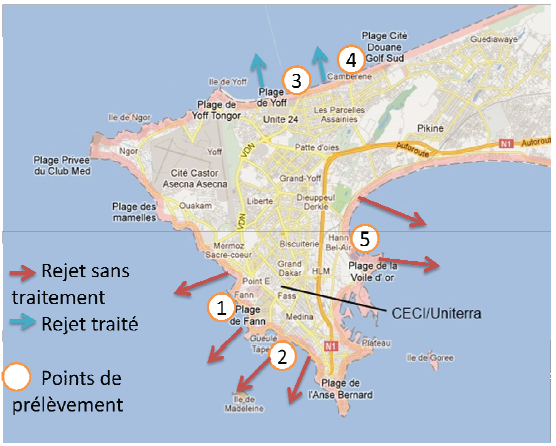
Les échantillons de sédiment ont été prélevés au mois d’octobre 2011 le long de la côte de Dakar au niveau de cinq points d’évacuation des eaux usées vers la mer. Les sites 1 et 2 correspondent aux points de rejet d’eaux usées domestiques brutes, les sites 3 et 4 aux points de rejet d’eaux traitées par la station d’épuration et le site 5 au point de rejet d’eaux usées industrielles et domestiques non traitées (Figure 1).
Figure 1
Carte de prélèvement avec les différents points d’évacuation des eaux usées.
Sampling locations and the various points of wastewater discharge.
Les sédiments ont été prélevés en surface par raclage dans des tubes de 200 mL qui sont remplis au plein. Au laboratoire, la couche superficielle du sédiment potentiellement oxydée par l’oxygène est éliminée et une partie du sédiment est séchée sous hotte à flux laminaire puis broyée dans un mortier et tamisée à 63 µm afin d’obtenir la fraction fine. Cette dernière qui contient essentiellement les métaux lourds est utilisée pour la détermination du carbone organique particulaire et des éléments métalliques.
2.2 Techniques analytiques
Le pH a été mesuré in situ dans l’eau par potentiométrie à l’aide d’une électrode de verre combinée à une électrode référence Ag/AgCl, [KCl] = 3M. L’électrode de mesure a été introduite dans le sédiment et la lecture est faite après stabilisation de l’appareil. L’alcalinité, qui correspond à la quantité d’acide nécessaire à la neutralisation des bases présentes dans l’échantillon, est déterminée par titrage potentiométrique avec de l’acide chlorhydrique 0,02M à l’aide d’un titrateur automatique (Metrohm modèle Titrino 736GP) après extraction de l’eau par centrifugation.
L’analyse granulométrique des sédiments est effectuée à l’aide d’un granulomètre laser (Malvern Master-sizer 2000). En fonction de la taille de leurs particules, les sédiments sont classés en deux groupes : les sédiments grossiers (diamètre > 63 µm) constitués de gravier (diamètre > 2 mm) et de sable (63 µm < diamètre < 2 mm) et les sédiments fins (diamètre < 63 µm) composés de silt (2 µm < diamètre < 63 µm) et d’argile (diamètre < 2 µm) (BELLAIR et POMEROL, 1977). La teneur en eau est déterminée par différence pondérale avant et après séchage du sédiment frais sous hotte à flux laminaire à la suite de la stabilisation de la masse. Le carbone total particulaire, l’azote et le soufre sont déterminés sur la fraction 63 µm du sédiment à l’aide d’un analyseur élémentaire (CHNS Thermo Scientific, Flash 2000) équipé d’un détecteur interne TCD. La calibration de l’appareil s’est faite avec un standard de sol et l’oxydation se fait à 950 °C. Le carbone organique est estimé en faisant la différence entre le carbone total et le carbone inorganique obtenu après calcination du sédiment à 450 °C pendant 24 h, ce qui permettait d’éliminer la matière organique.
Les éléments métalliques totaux du sédiment sont analysés à l’ICP-OES (Thermo Scientific, iCAP 6000 Séries) et l’ICP-MS (Varian 820-MS) après minéralisation totale de la fraction sédimentaire 63 µm. Cette attaque est effectuée selon le protocole proposé par OUDDANE (1990) et modifié par BILLON (2001). Environ 200 mg de sédiment sont introduits dans un réacteur en téflon et on a ajouté 5 mL d’acide fluorhydrique 40 %, 5 mL d’acide chlorhydrique 37 % et 2,5 mL d’acide nitrique 69 %. La minéralisation est effectuée au micro onde (CEM Corporation, Mars 5 x-pres) à 180 °C pendant 25 minutes et la neutralisation de l’acide fluorhydrique se fait en ajoutant de l’acide borique 4 %. À la fin de la neutralisation, le minéralisât est versé dans un tube en téflon de 50 mL qui est complété avec de l’eau ultra pure au volume puis filtré. Cette procédure a été validée en pratiquant la même extraction sur un sédiment standard certifié HISS-1 (Conseil national de recherches du Canada, matériaux de référence certifiés, sédiments marins) et les résultats obtenus sont comparés aux valeurs certifiées dans le tableau 1.
Tableau 1
Valeurs mesurées et certifiées des éléments traces métalliques (mg•kg-1) du sédiment standard certifié HISS1-1.
Measured and certified concentrations of trace metals (mg•kg-1) in the sediment standard reference material HISS1-1.
3. Résultats et discussion
Les paramètres mesurés sont résumés dans le tableau 2. Les valeurs de pH dans les cinq sites sont basiques variant de 9,02 à 9,66 avec une moyenne de 9,2 ± 0,27. Les eaux interstitielles présentent une alcalinité variant de 7 mmoles•L-1 à 9,6 mmoles•L-1 avec une moyenne de 8,52 ± 1,02. Il existe une corrélation positive entre le pH et l’alcalinité.
Tableau 2
Paramètres physicochimiques et teneur en métaux lourds des sédiments.
Physicochemical characteristics and trace metal concentrations in sediment samples.
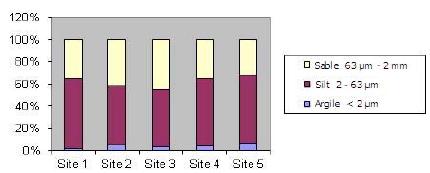
La distribution granulométrique des sédiments est représentée dans la figure 2. Elle montre que la fraction inférieure à 63 µm est dominante, variant entre 55 et 65 % en fonction des sites. Nos sédiments semblent donc homogènes de par leur texture, ce qui réduirait les éventuels artéfacts d’origine physique.
Figure 2
Répartition granulométrique des sédiments.
Size distribution of the sediments.
L’analyse élémentaire montre que nos échantillons sont pauvres en carbone organique avec une teneur moyenne de 0,12 ± 0,04 %. La détermination du rapport C/N donne une valeur moyenne de 24,9 ± 8,4. À l'équilibre, un rapport C/N compris entre 6 et 7 correspondrait au phytoplancton marin frais. Dans nos sédiments, ce rapport varie entre 12,6 et 33,2, suggérant la présence de matières organiques relativement anciennes et réfractaires comme les substances humiques. Ce rapport élevé indique également une origine de la matière organique probablement terrigène (SUFFET et MCCARTHY, 1987). Le ratio S/C montre une certaine disparité entre les sites avec des valeurs très faibles qui varient de 0,12 (site 3) à 0,69 (site 5) donnant une moyenne de 0,27 ± 0,24. Ces données suggèrent, d’une part, que la plupart du temps, le dépôt du sulfure dans nos sédiments se fait en condition oxique (MORSE et BERNER, 1995) et, d’autre part, témoignent d’une oxygénation suffisante de l’interface eau/sédiment. Par ailleurs, les ratios C/N et S/C obtenus dans notre étude sont comparables à ceux obtenus par MBASSANI et al. (2003) au niveau de la plate-forme atlantique sénégalaise avec des valeurs moyennes respectives de 23 et 0,36 avec les mêmes disparités que nous avons notées.
Les teneurs en éléments traces métalliques des sédiments par attaque totale montrent que le Cd et le Pb ont des concentrations très fortes par rapport aux valeurs obtenues par KIKOUAMA et al. (2009) à Dakar dans le kaolin (Tableau 2). Les autres éléments présentent des teneurs moins importantes. Pour évaluer le niveau de pollution des sédiments, nous avons déterminé un certain nombre de paramètres de qualité qui sont le facteur d’enrichissement, l’indice de pollution sédimentaire (IPS) et l’indice de charge de pollution (PLI).
3.1 Facteur d’enrichissement
Les métaux sont principalement associés aux particules fines (argiles, oxydes et hydroxydes de fer, matières organiques, sulfures, etc.), et il serait donc nécessaire d’exprimer les concentrations des éléments traces métalliques (ETM) en fonction d’un paramètre lié à la granulométrie des sédiments. Pour cela, nous avons choisi de normaliser les concentrations des ETM mesurées par rapport à l’aluminium, constituant majeur des minéraux argileux, et qui s’avère être un bon traceur de la fraction fine. De plus, cet élément se trouve en fortes concentrations dans les sédiments de sorte qu’un enrichissement artificiel lié à un apport anthropique est peu probable et étant donné qu’il est un élément réfractaire, sa diffusion massive vers l’eau ne se produit pas. Cette normalisation, qui consiste à exprimer le ratio de la teneur d’une substance donnée par rapport à celle du facteur normalisant, ici Al, permet ainsi de définir le facteur d’enrichissement FE d’un élément trace métallique donné dans le sédiment. Ce facteur d’enrichissement est exprimé par la formule suivante (Équation ) :
Les facteurs d’enrichissement calculés (Tableau 3) pour nos sites montrent une forte contamination en Cd et en Pb (FEmoyen Cd = 23 et FEmoyen Pb = 86) et un faible enrichissement pour les autres éléments par rapport aux valeurs de fond géologiques produites par KIKOUAMA et al. (2009). Selon la classification de SAKAN et al. (2009), les sites 1, 2, 3 et 4 sont sévèrement contaminés en Cd (10 < FECd < 25) et le site 5 est très sévèrement enrichi (25 < FECd < 50); pour l’enrichissement en Pb, le site 1 est très sévèrement enrichi (25 < FEPb < 50), les autres sites montrent une contamination extrêmement sévère (FEPb > 50). Cet enrichissement témoigne d’une forte pollution, d’où l’intérêt de faire un carottage pour étudier l’historique de cette pollution. S’agissant du Cu, Cr, Ni et Zn, les sites 1, 2, 3 et 4 présentent un enrichissement modéré (5 < FE < 10); par contre, le site 5 donne une contamination modérément sévère. D’après ZHANG et LIU (2000), un FE compris entre 0,05 et 1,5 indique que le métal est entièrement cristallisé dans le sédiment alors qu’un FE supérieur à 1,5 suggère une origine anthropique. Dans cette étude, la moyenne des FE de tous les métaux est supérieure à 1,5, suggérant l’origine anthropique des métaux dans le sédiment.
Tableau 3
Facteur d’enrichissement (FE) et Indice de Pollution Sédimentaire (IPS) des sites étudiés.
Enrichment factor (EF) and Sediment Pollution Index (SPI) for sediments from the studied sites.
3.2 Indice de pollution sédimentaire
Le calcul des facteurs d’enrichissement a permis d’établir un classement de nos sédiments en fonction de leur contamination métallique mais il ne prend pas en compte la notion de toxicité liée à chaque métal. Ainsi, RUBIO et al. (2000) ont introduit l’indice de pollution sédimentaire (IPS) qui est la somme linéaire de FE prenant en compte la toxicité relative de chaque métal en lui affectant un facteur pondérateur. Un poids de 1 est assigné à Cr et Zn, 2 à Cu et Ni, 5 à Pb et 300 à Cd (RUBIO et al., 2000; SINGH et al., 2002). Ainsi, IPS peut être exprimé par la formule suivante (Équation 2) :
avec :
FEm : facteur d’enrichissement du métal m;
Wm : poids de toxicité ou facteur pondérateur du métal m.
L’IPS s’accompagne de cinq classes de pollution qui se repartissent entre le sédiment sain (0 < IPS < 2) et le sédiment dangereux (IPS > 20) (SINGH et al., 2002). Sur la base de cette classification, les sites 1, 2 et 3 sont fortement pollués (10 < IPS < 20) alors que les sites 4 et 5 sont dangereux (IPS > 20) (Tableau 3). Ainsi, nos sites peuvent être classés par ordre croissant de pollution de manière suivante : site 3 – site 1 – site 2 – site 4 – site 5. Ce classement montre que la station d’épuration ne parvient pas à traiter toutes les eaux usées, ce qui peut expliquer l’IPS élevé (21,4) du site 4; par contre, l’IPS 49,7 du site 5 témoigne du déversement des eaux industrielles non traitées dans ce milieu. Les fortes pollutions notées dans les sites 1, 2 et 3 peuvent s’expliquer par le non-traitement des eaux usées urbaines qui y sont rejetées. En outre, le Cd et le Pb contribuent respectivement à l’IPS à l’ordre 93 % et 6 %; les autres éléments ne représentent que 1 % de cet indice.
3.3 Pollution Load Index (PLI)
Pour mettre en exergue l’impact des activités urbaines sur la qualité des sédiments, l’indice de charge de pollution (PLI) introduit par TOMLINSON et al. (1980) est déterminé selon la relation suivante (Équation 3) :
Dans ce travail, Cr, Cu, Cd, Ni, Pb et Zn ont fait l’objet d’une évaluation, ce qui fait que n = 6. Les valeurs de PLI calculées pour les sites 1, 2, 3, 4 et 5 sont respectivement 8; 14; 6; 6 et 24. Ces résultats sont en corrélation avec les valeurs d’IPS obtenues (Figure 3). Ce graphique suggère que plus la charge de pollution est importante, plus le sédiment est pollué. Cependant, il est judicieux de souligner la valeur élevée de R2 (0,82) qui est peut-être trompeuse, d’autant plus qu’elle est surtout influencée par la forte valeur de l’IPS notée au site 5 et due aux rejets industriels. Néanmoins, la charge de pollution est proportionnelle à la quantité d’eaux usées rejetées, donc à l’urbanisation, ce qui confirme les indices obtenus dans nos sites à l’exception du site 5 où on peut constater que l’urbanisation est moins importante mais les activités industrielles sont dominantes.
Figure 3
Pollution sédimentaire vs. charge de pollution urbaine.
Sediment pollution vs. urban pollution load.
3.4 Relation entre éléments
Le tableau 4 présente la matrice des coefficients de corrélation des métaux lourds dans les sédiments de la zone urbaine de Dakar. Des corrélations positives élevées et modérées sont observées entre Pb/Cd, Pb/Co, Cr/Cu, Cr/Zn, Cr/Fe, Cr/Mn, Cu/Ni, Cu/Fe, Cu/Mn et Zn/Mn, indiquant leurs sources communes possibles à partir des activités industrielles et/ou urbaines ainsi que des comportements comparables dans le sédiment. Par ailleurs, en condition oxique, les hydroxydes de Fe et de Mn sont sous une forme oxydée influençant de manière importante le comportement de certains métaux dans les écosystèmes aquatiques (HOROWITZ, 1991). Les corrélations négatives notées avec le Fe et le Mn vis-à-vis du Cd, Co et Pb montrent que ces hydroxydes ont précipité ces éléments au sein du sédiment. De plus, les teneurs faibles de nos sédiments en carbone organique peuvent expliquer que les hydroxydes de Fe et de Mn seraient les principales phases fixatrices des métaux d’autant plus qu’il s’agit de sédiment de surface donc les sulfures seront sous forme oxydée ne pouvant pas ainsi piéger les métaux.
Tableau 4
Corrélation entre les éléments métalliques dans le sédiment.
Inter-element correlation matrix for trace metals in sediments.
4. Conclusion
L’évaluation de la qualité des sédiments a été effectuée par le calcul de divers indices. Un enrichissement important des sédiments en cadmium et en plomb a été surtout noté. L’IPS qui estime le degré de contamination d’un site en fonction de la toxicité relative de chaque métal considéré fait état d’une forte pollution, voire même d’une dangerosité des sédiments étudiés. En effet, le cadmium et le plomb, présents en fortes teneurs dans les sites, contribuent respectivement de l’ordre de 94 % et 5 % à la dangerosité potentielle des sédiments (selon le classement de l’indice de pollution sédimentaire) alors que le zinc, le cuivre, le nickel et le chrome, également présents en fortes concentrations, ne représentent que 1 % de la pollution globale. Cet indice élevé, qui a permis de classer les sites par ordre croissant de pollution, n’est pourtant pas forcément un signe de toxicité réelle vis-à-vis des organismes benthiques présents dans les sédiments. Il s’avère donc nécessaire d’évaluer la toxicité des métaux par des études qui vont prendre en compte leur biodisponibilité, car ils peuvent être piégés par les sulfures, et de confirmer par des bioessais. Par ailleurs, les données du PLI montrent que cette contamination est principalement due aux activités humaines et industrielles.
Parties annexes
Références bibliographiques
- AHN J.S., Y.S. PARK, J.Y. KIM et K.W. KIM (2005). Mineralogical and geochemical characterization of arsenic in an abandoned mine tailings of Korea. Environ. Geochem. Health, 27, 147-157.
- BELLAIR P. et C. POMEROL (1977). Eléments de géologie. Armand Colin, Paris, France, 528 p.
- BILLON G. (2001). Géochimie des métaux et du soufre dans les sédiments des estuaires de la Seine et de l'Authie. Thèse de Doctorat, Univ. Lille 1, Lille, France, 230 p.
- BOENING D.W. (1999). An evaluation of bivalves as biomonitors of heavy metals pollution in marine waters. Environ. Monitor. Assess., 55, 459-470.
- BOUGHRIET A., N. PROIX, G. BILLON, P. RECOURT et B. OUDDANE (2007). Environmental impacts of heavy metal discharges from a smelter in Deûle-canal sediments (Northern France): concentration levels and chemical distribution. Water Air Soil Pollut., 180, 83-95.
- D’ADAMO R., M. DI STASIO et A. FABBROCHINI (2008). Migratory crustaceans as biomonitors of metal pollution in their nursery areas. The Lesina lagoon (SE Italy) as a case study. Eviron. Monitor. Assess., 143, 15-24.
- DABY D. (2006). Coastal pollution and potential biomonitors of metals in Mauritius. Water Air Soil Pollut., 174, 63-91.
- GAYE M. et S. NIANG (2002). Politique d’assainissement au Sénégal et épuration des eaux usées. Édition ENDA, Dakar, Sénégal, 42 p.
- HOROWITZ A.J. (1991). A primer on sediment-trace element chemistry. Lewis Publishers, Chelsea, MI, U.S.A., 136 p.
- HUANG H., J.Y. WU et J.H. WU (2007). Heavy metal monitoring using bivalved shellfish from Zhejiang coastal waters, East China Sea. Environ. Monitor. Assess., 129, 315-320.
- KIKOUAMA ODILON J.R., K.L. KONAN, A. KATTY, J.P. BONNET, L. BALDÉ et N. YAGOUBI (2009). Physicochemical characterization of edible clays and release of trace elements. Appl. Clay Sci., 43, 135-141.
- LEE M.R. et J.A. CORREA (2005). Effect of copper mine tailings disposal on littoral meiofaunal assemblages in the Atacama region of Northern Chile. Mar. Environ. Res., 59, 1-18.
- MBASSANI NZOUSSI P., J.R. DISNAR et F. LAGGOUN-DE´FARGE (2003). Organic matter characteristics of Cenomanian-Turonian source rocks: implications for petroleum and gas exploration onshore Senegal. Mar. Petrol. Geol., 20, 411-427.
- MEMET V. et S. BÜLENT (2012). Assessment of nutrient and heavy metal contamination in surface water and sediments of the upper Tigris River, Turkey. Catena, 92, 1-10.
- MORSE W.J. et A.R. BERNER (1995). What determines sedimentary C/S ratio. Geochim. Cosmochim. Acta, 59, 1073-1077.
- OIS (Observatoire des Industries du Sénégal) (2010). Répartition régionale des industries en 2000. http://www.obs-industrie.sn/PRI(extrait).htm (consulté le 27/04/2010).
- ONAS (Office National de l’Assainissement du Sénégal) (2005). Rejet en mer des eaux usées à Dakar. http://www.onas.sn/joomla/index.php?option=com_content&view=article&id=1%3Apresentation-de-la-step-de-camberene&Itemid=48&lang=fr (consulté le 25/02/2010).
- OUDDANE B. (1990). Comportement des éléments majeurs et mineurs dans un milieu soumis à des gradients physico-chimiques marqués : cas de l'estuaire de la Seine. Thèse de Doctorat, Univ. Lille 1, Lille, France, 227 p.
- RAO J.V., P. KAVITHA, K. SRIKANTH, P.K. USMAN et T.G. RAO (2007). Environmental contamination using accumulation of metals in marine sponges, Sigmadocia fibulata inhabiting the coastal waters of Gulf of Mannar, India. Toxicol. Environ. Chem., 89, 487-498.
- ROYCHOUDHURY A.N. et M.F. STARKE (2006). Partitioning and mobility of trace metals in the Blesbokspruit: impact assessment of dewatering of mine waters in the East Rand, South Africa. Appl. Geochem., 21, 1044-1063.
- RUBIO B., M.A. NOMBELA et F. VILAS (2000). Geochemistry of major and trace elements in sediments of the Ria de Vigo (NW Spain): an assessment of metal pollution. Mar. Pollut. Bull., 40, 968-980.
- SAKAN S.M., D.S. DJORDJEVIC, D.D. MANOJLOVIC et P.S. POLIC (2009). Assessment of heavy metal pollutants accumulation in the Tisza River sediments. J. Environ. Manage., 90, 3382-3390.
- SINGH M., G. MÜLLE et I.B. SINGH (2002). Heavy metals in freshly deposited stream sediments of rivers associated with urbanisation of the Ganga plain, India. Water Air Soil Pollut., 141, 35-54.
- SMOLDERS R., L. BERVOETS, V. WEPENER et R. BLUST (2003). A conceptual framework for using mussels as biomonitors in whole efflent toxicity. Hum. Ecol. Risk Assess., 9, 741-760.
- SUFFET I.H. et P. MACCARTHY (1987). Aquatic humic substances. Vol 219, American Chemical Society, Washington, DC, USA, 864 p.
- SULTAN K., A.S. NOOR et P. STEFAN (2011). Distribution of Pb, As, Cd, Sn and Hg in soil, sediment and surface water of the tropical river watershed, Terengganu (Malaysia). J. Hydro-Environ. Res., 5, 169-176.
- TOMLINSON D.C., J.G. WILSON, C.R. HARRIS et D.W. JEFFERY (1980). Problems in the assessment of heavy metals levels in estuaries and the formation of a pollution index. Helgol. Wiss. Meeresunters, 33, 566-575.
- XUELU G., A.C. CHEN-TUNG (2012). Heavy metal pollution status in surface sediments of the coastal Bohai Bay. Water Res., 46, 1901-1911.
- ZHANG J et C.L. LIU (2000). Riverine composition and estuarine geochemistry of particulate metals in China-weathering features, anthropogenic impact and chemical fluxes. Estuar. Coast. Shelf Sci., 54, 1051-1070.
Liste des figures
Figure 1
Carte de prélèvement avec les différents points d’évacuation des eaux usées.
Sampling locations and the various points of wastewater discharge.
Figure 2
Répartition granulométrique des sédiments.
Size distribution of the sediments.
Figure 3
Pollution sédimentaire vs. charge de pollution urbaine.
Sediment pollution vs. urban pollution load.
Liste des tableaux
Tableau 1
Valeurs mesurées et certifiées des éléments traces métalliques (mg•kg-1) du sédiment standard certifié HISS1-1.
Measured and certified concentrations of trace metals (mg•kg-1) in the sediment standard reference material HISS1-1.
Tableau 2
Paramètres physicochimiques et teneur en métaux lourds des sédiments.
Physicochemical characteristics and trace metal concentrations in sediment samples.
Tableau 3
Facteur d’enrichissement (FE) et Indice de Pollution Sédimentaire (IPS) des sites étudiés.
Enrichment factor (EF) and Sediment Pollution Index (SPI) for sediments from the studied sites.
Tableau 4
Corrélation entre les éléments métalliques dans le sédiment.
Inter-element correlation matrix for trace metals in sediments.