Corps de l’article
Les antigènes de groupes sanguins Rh (Rhésus) sont portés par un complexe protéique composé de deux sous-unités principales spécifiquement exprimées dans le lignage érythrocytaire, Rh et RhAG (Rh-associated glycoprotein), codées respectivement par des gènes homologues présents sur le bras court des chromosomes 1 (p34-p36) et 6 (p12-p21). Des protéines accessoires (LW/ICAM-4, CD47 et glycophorine B) sont également associées à ce complexe. Dans le phénotype Rhnull - caractérisé par une anémie hémolytique de sévérité variable associée à une stomato-sphérocytose - le complexe Rh est absent ou sévèrement diminué. Le rôle structural majeur du complexe Rh dans la membrane du globule rouge résulte d’une interaction spécifique avec l’ankyrine R, permettant l’ancrage des protéines du squelette membranaire dépendant de la spectrine. Des mutations du gène RH ou du gène RHAG sont à l’origine des phénotypes Rhnull. Parmi ces mutations, l’une d’entre elles, affectant le gène RHAG, abolit l’interaction avec l’ankyrine [1].
Les protéines Rh appartiennent à la superfamille des transporteurs d’ammonium
Des progrès importants ont été réalisés dans la connaissance de la structure et du polymorphisme des protéines Rh. Cependant, bien que les prévisions de structure secondaire aient été en faveur d’une organisation topologique avec 12 domaines transmembranaires, évocatrice de celle des protéines de transport, la fonction des protéines Rh est longtemps restée mystérieuse. La première indication a trouvé son origine dans des études phylogénétiques qui ont révélé que les protéines de la famille Rh, incluant les protéines érythroïdes (Rh, RhAG) et des homologues non érythroïdes (RhBG et RhCG) présents dans divers tissus, présentent une relation ancestrale avec des transporteurs spécifiques d’ammonium de la famille Mep/Amt (methylammonium permease/ammonium transporters) conservés chez les archaebactéries, les eubactéries, les champignons, les végétaux, ainsi que chez des animaux invertébrés, définissant ainsi la superfamille des protéines Mep/Amt/Rh. La preuve expérimentale a été apportée par des expériences de complémentation fonctionnelle montrant que RhAG et RhCG peuvent restaurer l’influx et l’efflux d’ammonium dans des levures déficientes pour les trois transporteurs endogènes Mep1, Mep2 et Mep3 [2]. RhAG et RhCG seraient donc les premiers transporteurs spécifiques d’ammonium décrits chez les vertébrés. Des travaux ultérieurs fondés sur l’expression dans des oeufs de xénope ont confirmé que les glycoprotéines Rh (RhAG, RhBG et RhCG) sont toutes capables de transporter l’ammonium.
Dans les micro-organismes et chez les végétaux, l’ammonium représente une excellente source d’azote. Cependant, chez les vertébrés, l’ammonium est un dérivé du catabolisme des protéines produit par l’intestin, le rein et les muscles, et éliminé par le foie. Il est toxique pour le système nerveux. Son élimination contrôlée dans l’urine joue un rôle majeur dans la régulation de l’équilibre acide-base. Les glycoprotéines humai-nes RhBG et RhCG sont majoritairement exprimées dans le rein, mais elles sont également présentes dans le foie (et aussi dans la peau et les gonades), organes impliqués dans la production et l’élimination de l’ammonium.
Mécanismes de transport d’ammonium
L’ammonium existe en solution sous deux formes en équilibre, NH4+ et NH3, dont la concentration est dépendante du pH (pKa = 9,25 à 22° C). Classiquement, il est admis que la forme neutre NH3 est capable de diffuser de façon passive à travers les lipides membranaires alors que le transport de la forme chargée NH4+ est assuré de manière non spécifique par différents transporteurs de K+ et de Na+. Des études indirectes fondées sur l’incorporation de l’analogue méthylammonium et d’autres plus directes d’électrophysiologie (voltage-clamp) ont abouti à des conclusions contradictoires concernant le mécanisme de transport relayé par les glycoprotéines Rh exprimées dans des oeufs de xénope. Pour certains, il s’agirait d’un transport électrogénique et, pour d’autres, d’un transport électroneutre relayé par un échangeur NH4+/H+, sans pouvoir toutefois exclure formellement un mécanisme fonctionnellement équivalent de transport net de NH3. Il est important de déterminer laquelle des deux formes de l’ammonium traverse la membrane, celle chargée (ion NH4+) ou neutre (gaz NH3), car des transporteurs disctints seraient impliqués ; en outre, ces molécules pourraient jouer un rôle de médiateur réglant l’activité de différents transporteurs (canal ENaC, échangeurs Cl-/HCO3-) et l’implication dans une telle cascade de signalisation pourrait donner aux glycoprotéines Rh, outre la fonction de transport d’ammonium, une fonction de récepteurs sensibles à l’ammonium.
Transport d’ammonium dans les globules rouges
Les globules rouges représentent un bon système pour explorer les mécanismes de transport d’ammonium et plus particulièrement la fonction de RhAG dans son contexte naturel. On sait que la membrane du globule rouge est extrêmement perméable au gaz NH3, mais pas aux ions NH4+. Nous avons récemment mis à profit l’existence de variants génétiques humains et murins présentant divers déficits des protéines qui composent ou interagissent avec le complexe Rh, pour explorer leur impact sur la fonction de transport d’ammonium des globules rouges [3]. Comme les mouvements de NH3 à travers les membranes plasmiques sont très rapides, la mesure du transport a été réalisée par spectrophotométrie en flux interrompu (stopped-flow) permettant d’analyser en quelques fractions de seconde les variations de pH intracellulaire de stromas érythrocytaires contenant une sonde fluorescente dépendante du pH, soumis à des gradients d’ammonium ou de méthylammonium dans des conditions iso-osmotiques (Figure 1). Schématiquement, une entrée de NH3 se traduira par une alcalinisation cellulaire alors que l’entrée de NH4+ entraînera une acidification. Dans tous les cas, on observe une alcalinisation rapide, correspondant à une protonation de NH3 ou de CH3NH2, suivie par un retour au pH du milieu d’incubation. Les résultats indiquent que, par rapport aux témoins, les cellules humaines déficientes pour une ou plusieurs protéines du complexe Rh (Rhnull, LWnull, 4.2null), et les cellules murines respectivement déficientes en ankyrine (souris nb/nb) ou en spectrine (souris sph/sph) ayant un défaut associé d’expression de Rh et RhAG (Figure 1), présentent une diminution de la perméabilité au NH3/CH3NH2 qui est strictement corrélée à leur déficit en protéine RhAG, mais n’est pas affectée par une réduction de l’expression des autres protéines du complexe (RhD ou RhCcEe, CD47 ou LW). Par conséquent, bien qu’il existe une entrée basale de NH3/CH3NH2 par diffusion lipidique chez les variants Rhnull et les autres variants cellulaires humains et murins, ces résultats indiquent que la protéine RhAG accélère l’influx cellulaire de NH3.
Figure 1
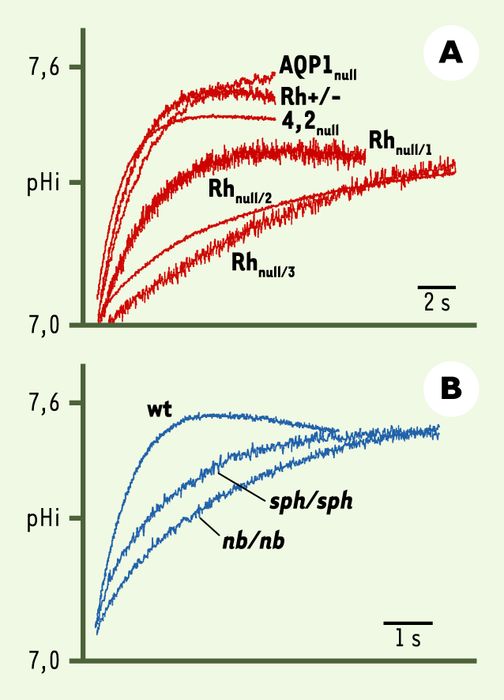
Transport de NH3 dans les stromas érythrocytaires déficients en protéine RhAG.
Les cinétiques de variation du pH intracellulaire (pHi) sont déterminées dans des stromas érythrocytaires refermés (contenant de la pyranine) soumis à un gradient entrant de méthylammonium (32,5 mM, pH 7,0, 15° C). Le pH intracellulaire est mesuré grâce à la variation de fluorescence de la pyranine à l’aide d’un spectrophotomètre de flux interrompu. Seule la phase initiale, très rapide, d’alcalinisation (due à l’influx de NH3) est représentée. A. Stromas érythrocytaires humains provenant de sujets RhD positif (Rh+), RhD négatif (Rh-), Rhnull de type régulateur (3 sujets), 4.2null, et AQP-1null. Tous les échantillons Rhnull reg ont un déficit en protéine RhAG. B. Stromas érythrocytaires provenant de souris sauvages (wt), et de souris nb/nb et sph/sph respectivement déficientes en ankyrine-R et en spectrine-α présentant un déficit associé en protéine RhAG (respectivement de 95 et 40 %) (d’après [3]).
La protéine RhAG : un canal à gaz
Une preuve supplémentaire en faveur d’un mécanisme RhAG-dépendant a été apportée en montrant que la perméabilité au NH3/CH3NH2 est sensible aux dérivés mercuriels (réversible par le β-mercaptoéthanol) et qu’elle est réduite après protéolyse in situ de la protéine RhAG. La protéine RhAG serait donc l’une des premières protéines membranaires fonctionnant comme un canal à gaz, dont la conductance approximative (gradient 1 M d’ammonium, pH 7) a été estimée à 2x106 molécules NH3 /s par complexe Rh.
Une contribution essentielle a été apportée par d’autres travaux très récents qui ont révélé la structure cristallographique 3D à haute résolution du transporteur d’ammonium AmtB de E. coli [4, 5]. Ces études ont montré que chaque sous-unité du complexe trimérique AmtB présente la même conformation en présence et en l’absence de substrat (ammonium et méthylammonium), suggérant que cette protéine fonctionne comme un canal plutôt que comme un transporteur, car un mécanisme de transport implique classiquement l’existence de différents états de conformation induits par la translocation du substrat. L’analyse de la structure 3D a révélé schématiquement que le canal, localisé au centre de chaque monomère AmtB (Figure 2), comprend à son sommet un vestibule extracellulaire bordé par des acides aminés aromatiques où NH4+/NH3 peuvent se fixer, suivi d’un pore hydrophobe étroit où, à la suite d’une déprotonation, NH3 seul peut diffuser en établissant des liaisons hydrogène avec deux résidus histidine. Le canal se termine sur la face cytoplasmique par un vestibule où se rétablit l’équilibre entre NH3 et NH4+ [4, 5]. Clairement, le canal n’autorise pas la translocation de protons et le transport serait donc non électrogénique. En outre, une étude fonctionnelle par spectrophométrie en flux interrompu, analogue à celle décrite pour RhAG, a permis de montrer qu’après reconstitution dans des protéoliposomes la protéine AmtB purifiée se comporte comme un canal à NH3 [4]. La comparaison des séquences montre également que les résidus aromatiques et les histidines qui bordent le canal AmtB sont conservées dans les glycoprotéines Rh, mais pas dans les protéines RhD et RhCcEe. Ces études structurales et fonctionnelles suggèrent que les protéines de la famille Mep/Amt/Rh fonctionneraient de manière identique, bien que des études complémentaires soient nécessaires pour étayer cette hypothèse.
Figure 2
Le canal NH3 du transporteur d’ammoniaque AmtB de E. coli.
L’analyse de la structure cristallographique à haute résolution (1,5 Å) du transporteur AmtB de E. coli a permis de mettre en évidence la présence dans chaque sous-unité de la protéine trimérique d’un pore central flanqué d’un vestibule plus large à l’entrée et à la sortie de la protéine [4, 5]. Le vestibule d’entrée est bordé par des acides aminés aromatiques (W148, F103, F107) qui stabilisent l’ion ammonium NH4+ (sphère orange) et permettent sa déprotonation. Le pore hydrophobe étroit (20 Å de long, cadre pointillé rouge) contient deux résidus d’histidine (en jaune, positions 168 et 318) qui stabilisent trois molécules de NH3 (sphères bleues) grâce à des liaisons hydrogène au cours de leur passage à travers le canal. Dans le vestibule de sortie, sur la face cytoplasmique, il y a retour à l’équilibre entre les formes neutres (NH3) et chargées (NH4+) (d’après [4] avec la permission de Science).
Les études antérieures suggérant que le transport associé aux glycoprotéines RhAG et RhCG est relayé par un échange électroneutre NH4+/H+ sont compatibles avec le mécanisme proposé de transport de NH3 pour au moins deux raisons : l’échange NH4+/H+ est fonctionnellement équivalent à un transport net de NH3, et il existe un site de fixation de NH4+ dans le vestibule externe du transporteur AmtB. Les autres études suggérant un mécanisme de transport électrogénique sont plus difficiles à interpréter. Cependant, elles ont été conduites dans les oeufs de xénope où ont été mis en évidence des courants endogènes induits par l’ammonium. Malgré cette limitation, il a été suggéré que RhCG jouerait un rôle spécifique dans le transport de NH4+ et de NH3 [6].
Rôle transporteur/canal des protéines Rh
Il convient de mentionner que d’autres travaux suggèrent que les protéines de la famille Rh pourraient fonctionner comme des transporteurs/canaux à CO2, car des mutants de Chlamydomonas reinhardtii n’exprimant plus la protéine Rh1 (paralogue de Rh dans l’algue verte) ne poussent que très lentement lorsqu’ils sont cultivés dans une atmosphère riche en CO2 [7]. La possibilité que les protéines Rh puissent transporter NH3 et CO2 reste donc à explorer. Bien que matière à débat, diverses études suggèrent que le canal hydrique AQP-1 est une protéine également perméable aux gaz CO2 et NH3.
L’importance physiologique de protéines perméables au gaz n’est pas évidente, mais on peut faire l’hypothèse selon laquelle elles seraient utiles dans des conditions exigeant des échanges extrêmement rapides, par exemple lorsque le temps de transit des cellules sanguines dans un organe est très réduit ou bien lorsque la membrane cellulaire présente une très faible perméabilité intrinsèque aux gaz. Dans les globules rouges, la protéine RhAG pourrait acheminer l’ammonium vers des organes de détoxification (foie, rein). Dans le rein, les glycoprotéines RhBG et RhCG, qui sont exprimées respectivement aux pôles basolatéral et apical des cellules intercalaires a des canaux collecteurs, pourraient coopérer fonctionnellement pour assurer la sécrétion de NH3, permettant de neutraliser les protons sécrétés (excrétion de NH4+ dans l’urine), et jouer ainsi un rôle important dans l’équilibre acide-base.
Conclusions
Les résultats acquis récemment ajoutent une nouvelle facette à la complexité des protéines de la famille Rh en soulignant leur capacité fonctionnelle de faciliter la diffusion de NH3, dont l’impact physiologique dans des conditions normales et pathologiques devra être exploré. Le développement de modèles murins d’inactivation génique devrait permettre de mieux comprendre les fonctions intégrées de ces protéines dans les divers organes où elles s’expriment.
Parties annexes
Références
- 1. Nicolas V, Le Van Kim C, Gane P, et al. Rh-RhAG/ ankyrin-R, a new interaction site between the membrane bilayer and the red cell skeleton, is impaired by Rh(null)-associated mutation. J Biol Chem 2003 ; 278 : 25526-33.
- 2. Marini AM, Matassi G, Raynal V, et al. The human Rhesus-associated RhAG protein and a kidney homologue promote ammonium transport in yeast. Nat Genet 2000 ; 26 : 341-4.
- 3. Ripoche P, Bertrand O, Gane P, et al. Human Rhesus-associated glycoprotein mediates facilitated transport of NH3 into red blood cells. Proc Natl Acad Sci USA 2004 ; 101 : 17222-7.
- 4. Khademi S, O’Connell J, Remis J, et al. Mechanism of ammonia transport by Amt/Mep/Rh : structure of AmtB at 1.35 A. Science 2004 ; 305 : 1587-94.
- 5. Zheng L, Kostrewa D, Berneche S, et al. The mechanism of ammonia transport based on the crystal structure of AmtB of Escherichia coli. Proc Natl Acad Sci USA 2004 ; 101 : 17090-5.
- 6. Bakouh N, Benjelloun F, Hulin P, et al. NH3 is involved in the NH4+ transport induced by the functional expression of the human RhCG glycoprotein. J Biol Chem 2004 ; 279 : 15975-83.
- 7. Soupene E, Inwood W, Kustu S. Lack of the Rhesus protein Rh1 impairs growth of the green alga Chlamydomonas reinhardtii at high CO2. Proc Natl Acad Sci USA 2004 ; 101 : 7787-92.
Liste des figures
Figure 1
Transport de NH3 dans les stromas érythrocytaires déficients en protéine RhAG.
Les cinétiques de variation du pH intracellulaire (pHi) sont déterminées dans des stromas érythrocytaires refermés (contenant de la pyranine) soumis à un gradient entrant de méthylammonium (32,5 mM, pH 7,0, 15° C). Le pH intracellulaire est mesuré grâce à la variation de fluorescence de la pyranine à l’aide d’un spectrophotomètre de flux interrompu. Seule la phase initiale, très rapide, d’alcalinisation (due à l’influx de NH3) est représentée. A. Stromas érythrocytaires humains provenant de sujets RhD positif (Rh+), RhD négatif (Rh-), Rhnull de type régulateur (3 sujets), 4.2null, et AQP-1null. Tous les échantillons Rhnull reg ont un déficit en protéine RhAG. B. Stromas érythrocytaires provenant de souris sauvages (wt), et de souris nb/nb et sph/sph respectivement déficientes en ankyrine-R et en spectrine-α présentant un déficit associé en protéine RhAG (respectivement de 95 et 40 %) (d’après [3]).
Figure 2
Le canal NH3 du transporteur d’ammoniaque AmtB de E. coli.
L’analyse de la structure cristallographique à haute résolution (1,5 Å) du transporteur AmtB de E. coli a permis de mettre en évidence la présence dans chaque sous-unité de la protéine trimérique d’un pore central flanqué d’un vestibule plus large à l’entrée et à la sortie de la protéine [4, 5]. Le vestibule d’entrée est bordé par des acides aminés aromatiques (W148, F103, F107) qui stabilisent l’ion ammonium NH4+ (sphère orange) et permettent sa déprotonation. Le pore hydrophobe étroit (20 Å de long, cadre pointillé rouge) contient deux résidus d’histidine (en jaune, positions 168 et 318) qui stabilisent trois molécules de NH3 (sphères bleues) grâce à des liaisons hydrogène au cours de leur passage à travers le canal. Dans le vestibule de sortie, sur la face cytoplasmique, il y a retour à l’équilibre entre les formes neutres (NH3) et chargées (NH4+) (d’après [4] avec la permission de Science).