Résumés
Résumé
Plusieurs interventions visent à réduire les surdoses aux opioïdes, dont la formation sur l’administration de la naloxone, un antidote permettant de renverser temporairement une surdose. Néanmoins, celles-ci ciblent davantage des personnes qui fréquentent les organismes de rue ou les cliniques spécialisées en dépendance. Moins nombreuses sont les initiatives ciblant les patients suivis en clinique de médecine familiale et traités avec des opioïdes pour la douleur chronique ou recevant un traitement par agonistes opioïdes (TAO) pour un trouble lié à l’usage des opioïdes. Cette étude à série temporelle visait à générer des données préliminaires sur l’efficacité d’une formation sur l’utilisation de naloxone chez les patients du groupe de médecine familiale universitaire (GMF-U) Charles-LeMoyne, en déterminant la rétention des concepts clés en lien avec les facteurs de risque, la reconnaissance et la prise en charge d’une surdose aux opioïdes. Les participants étaient des utilisateurs d’opioïdes (douleur chronique ou TAO) n’ayant pas suivi de formation antérieure sur la gestion des surdoses. L’intervention étudiée était une formation standardisée en petit groupe portant sur la gestion des surdoses aux opioïdes. L’instrument de mesure utilisé était le Opioid Overdose Knowledge Scale, un questionnaire validé et traduit de 14 questions totalisant 44 points. Il a été complété avant (T0), immédiatement après (T1) et 3 mois suivant la formation (T2) pour mesurer la rétention de l’information. Les pointages des 23 participants inclus étaient de 24,8/44 à T0, 39,1/44 à T1 et 35,0/44 à T2, suggérant une connaissance accrue et soutenue de la gestion des surdoses aux opioïdes dans les deux groupes. La majorité des participants formés se disaient confiants ou très confiants de savoir administrer la naloxone trois mois post-formation. Dans le contexte de la crise des opioïdes, la formation des patients à risque en médecine familiale est prometteuse et permettrait de rejoindre une population plus diversifiée d’utilisateurs d’opioïdes.
Mots-clés :
- naloxone,
- formation,
- douleur chronique,
- première ligne
Abstract
Various interventions exist to reduce opioid-related mortality, including Take Home Naloxone Programs. However, the overwhelming majority of these interventions are community programs targeting non-medical drug users. Only a few interventions target patients in primary care clinics taking prescription opioids for chronic pain or opioid agonist therapy (OAT) for opioid use disorder. The aim of this quasi-experimental time-series design study was to generate preliminary data on the effectiveness of an overdose prevention and naloxone training program in a primary care clinic setting. Study participants were opioid users (chronic pain or OAT) followed at Charles-LeMoyne family medicine group, who had no previous training on naloxone. The intervention was a standardized 1-hour group training session about overdose risk and management. A 14-question form used to evaluate naloxone training programs, the Opioid Overdose Knowledge Scale (OOKS), was used to assess the participant’s understanding and information retention. Means for OOKS scores were 24.8/44 at T0, 39.1/44 at T1 and 35.0/44 at T2, suggesting an increased and sustained knowledge regarding overdose management and naloxone use in both groups, following the training session. Most participants reported an increased confidence in their ability to use naloxone appropriately three months after the intervention. In the North American opioid crisis context, training at-risk patients in primary care clinics is promising and would allow reaching more opioid users to prevent opioid-related adverse events.
Keywords:
- naloxone,
- training,
- chronic pain,
- primary care
Resumen
Diversas intervenciones tienen como objetivo reducir las sobredosis de opioides, entre ellas la formación en administración de la naloxona, un antídoto que permite revertir temporalmente una sobredosis. Sin embargo, las mismas están destinadas más bien a las personas que frecuentan los organismos de calle o las clínicas especializadas en dependencia. Menos numerosas son las iniciativas destinadas a los pacientes que se sigue en clínica de medicina familiar y que son tratados con opioides por dolor crónico o que reciben un tratamiento de antagonistas opioides (TAO) por un problema relacionado con el uso de opioides. Este estudio de serie temporal está destinado a generar datos preliminares sobre la eficacia de una formación sobre lautilización de la naloxona entre los pacientes del grupo de medicina familiar universitaria Charles-LeMoyne, determinando la retención de los conceptos clave relacionados con los factores de riesgo, el reconocimiento y el tratamiento de una sobredosis de opioides. Los participantes eran usuarios de opioides (dolores crónicos o TAO) que no habían seguido una formación anterior sobre la gestión de las sobredosis. La intervención estudiada consistía en una formación normalizada por pequeños grupos, referida a las sobredosis de opioides. El instrumento de medida utilizado era el Opioid Overdose Knowledge Scale [escala de conocimiento de sobredosis de opioides], un cuestionario validado y traducido de 14 preguntas que totalizaban 44 puntos. Fue completado antes (T0), inmediatamente después (T4) y tres meses después de la formación (T1), con el objetivo de medir la retención de la información. Los puntajes de los 23 participantes incluidos fueron de 24,8/44 a T0, 39,1/44 à T1 y 35,0/44 à T2, lo que sugiere un conocimiento aumentado y sostenido de la gestión de las sobredosis de opioides en los dos grupos. La mayoría de los participantes declaraban tener confianza o mucha confianza en poder administrar la naloxona tres meses después de la formación. En el contexto de la crisis de los opioides, la formación de los pacientes a riesgo en medicina familiar es prometedora y permitiría alcanzar una población más diversificada de usuarios de opioides.
Palabras clave:
- naloxona,
- formación,
- dolor crónico,
- primera línea
Corps de l’article
Introduction
En 2015, les surdoses d’opioïdes étaient responsables de 118 000 décès à l’échelle mondiale (World Health Organization [WHO], 2018). Au Canada, 4 623 décès liés à la consommation d’opioïdes ont été recensés en 2018, ce qui en fait l’une des principales causes de décès accidentels au pays (Agence de la santé publique du Canada, 2020).
En moyenne, 101 visites aux urgences pour suspicion d’intoxication aux opioïdes ont été enregistrées mensuellement au Québec depuis 2016. De juillet 2017 à septembre 2020, 1 566 personnes sont décédées à la suite d’une intoxication suspectée aux opioïdes dans la province. La majorité de ces décès sont survenus chez des hommes âgés de 50 à 59 ans et étaient non intentionnels (Institut national de santé publique du Québec [INSPQ], 2021).
En Montérégie, 126 visites à l’urgence ont eu lieu en 2019 pour intoxication aux opioïdes. Cette même année, 39 décès avec suspicion d’intoxication aux opioïdes ont été recensés, dont 14 ont été confirmés à l’analyse toxicologique. Parmi les décès dont la cause a été confirmée comme une surdose, l’âge moyen était de 43 ans et les hommes étaient surreprésentés (70,0 %). De ces décès, 86,0 % sont survenus dans une résidence privée (Direction de la santé publique de la Montérégie, 2020).
Une des avenues pour diminuer la mortalité liée aux surdoses est de rendre les trousses de naloxone accessibles aux populations les plus à risque (Strang et al., 2014). Approuvée depuis plus de 45 ans au Canada, la naloxone (Narcan®) est un antidote sécuritaire et efficace qui prévient l’arrêt respiratoire associé à la surdose en renversant l’effet des opioïdes (Carter et Graham, 2013 ; Strang et al., 2019).
Depuis 2016, la naloxone est disponible gratuitement et sans prescription médicale au Québec, par injection intramusculaire ou par voie nasale (Institut national d’excellence en santé et services sociaux [INESSS], 2018). Il y a en moyenne 935 services de naloxone par mois dans les pharmacies communautaires du Québec depuis 2017. Le nombre de services est légèrement plus élevé chez les hommes âgés de 30 à 39 ans (INSPQ, 2021).
Formation sur la naloxone en milieux communautaires
L’Organisation mondiale de la Santé (OMS) recommande l’implantation de programmes d’accès communautaire à la naloxone depuis 2014 (Institut national de santé publique du Québec [INSPQ], 2017). C’est dans les organismes communautaires pour personnes faisant usage de drogues intraveineuses, particulièrement l’héroïne, que sont apparues les premières initiatives de réduction des méfaits avec la naloxone. Chez les populations consommant des drogues de rue, les programmes de formation sur la naloxone (Take Home Naloxone) ont, depuis 2001, largement fait leurs preuves comme étant une intervention efficace permettant de diminuer la mortalité liée aux surdoses avec peu d’effets secondaires (Mcdonald et Strang, 2016). En Colombie-Britannique, un vaste programme provincial communautaire (British Columbia Take Home Naloxone Program) a permis de renverser 1 580 surdoses d’avril 2016 à décembre 2017, selon des estimations récentes (Irvine et al., 2019).
À Montréal, la formation PRO-FAN (Prévention et réduction des surdoses – Formation et accès à la naloxone), mise sur pied en 2014 par le programme Cran (Centre de recherche et d’aide pour narcomanes), l’organisme communautaire Méta d’Âme et la Direction de la santé publique de Montréal, est un projet pilote de grande envergure qui vise à former les personnes qui consomment des opioïdes et leurs proches. La formation de six heures recrute des participants dans un contexte urbain (utilisation de drogues injectables notamment), ainsi que des pairs formateurs (Méta d’Âme, 2020).
Ces interventions ont aussi le potentiel d’augmenter le niveau de connaissance des participants, ainsi que leur en confiance en leur capacité à reconnaître et poser les gestes de premier secours en cas de surdose (Ashrafioun et al., 2016 ; Behar et al., 2015 ; Clark et al., 2014 ; Dietze et al., 2018 ; Enteen et al., 2010 ; Lopez Gaston et al., 2009 ; Mueller et al., 2015 ; Strang et al., 2008 ; Tobin et al., 2009). Certains programmes communautaires ont même rapporté une diminution des comportements à risque chez les participants à la suite de la formation et une augmentation d’initiation à un traitement par agonistes opioïdes (TAO) (Seal et al., 2005 ; Wagner et al., 2010).
Risque de surdose chez les patients traités pour la douleur chronique
Beaucoup moins nombreuses sont les études qui se sont intéressées au risque de surdose chez la population traitée avec des opioïdes pour une problématique de douleur chronique. Alors que les programmes initiaux de prévention ciblaient spécifiquement les utilisateurs de drogues de rue, les patients consommant des opioïdes prescrits pour traiter la douleur chronique présentent aussi une grande vulnérabilité aux surdoses, particulièrement lorsqu’ils ont des doses équivalentes à plus de 20 mg de morphine par jour (Adewumi et al., 2018).
Cette clientèle ne fréquente pas les ressources communautaires et présente plusieurs facteurs augmentant son risque de surdose aux opioïdes : un âge souvent avancé et des comorbidités telles que les troubles de santé mentale, les maladies respiratoires, la consommation d’alcool ou d’autres médicaments pouvant altérer l’état de conscience, lorsque combinés avec les opioïdes (Dunn et al., 2017 ; Mueller et al., 2016 ; Nielsen et al., 2018). De plus, la majorité des patients traités pour la douleur chronique ne connaissent pas leur risque de surdose ou le minimisent (Behar et al., 2016 ; Dunn et al., 2017 ; Mueller et al., 2016 ; Nielsen et al., 2018). Aux États-Unis, une étude dans une clinique de traitement de la douleur a démontré que 32,0 % des patients traités avaient développé des comportements de mésusage des opioïdes (Ives et al., 2006). Une autre étude dévoilait que 32,0 % des patients traités pour la douleur chronique avaient déjà utilisé leurs opioïdes en ne respectant pas la posologie recommandée (Behar et al., 2016).
En 2017, 3,5 millions de Canadiens ont été traités avec des opioïdes pour de la douleur, faisant du Canada le deuxième pays au monde avec la plus grande consommation d’opioïdes prescrits (Santé Canada, 2017 ; Strang et al., 2019). Bien qu’il soit difficile de documenter à quel point les opioïdes prescrits pour la douleur chronique jouent un rôle dans les surdoses accidentelles, la littérature démontre que le risque est probablement important. Au Canada, 28,0 % des surdoses investiguées entre 2016 et 2019 impliquaient des opioïdes pharmaceutiques (Agence de la santé publique du Canada, 2020). En Australie, parmi un échantillon de 208 patients traités pour la douleur chronique, 14,0 % ont manifesté des symptômes de surdoses telles que la somnolence ou la confusion (Nielsen et al., 2018). Finalement, aux États-Unis, 51 surdoses ont été recensées au sein d’une cohorte de 9 940 patients traités pour la douleur chronique (Dunn et al., 2010).
Prévention des surdoses en cliniques de médecine familiale : prescrire la naloxone avec les opioïdes
La majorité des cliniques de médecine familiale au Canada traitent des patients pour la douleur chronique alors que certaines cliniques offrent également le TAO. Depuis 2016, le Center for Disease Control (CDC) américain suggère de prescrire la naloxone chez les patients consommant chroniquement des opioïdes et présentant les facteurs de risque de surdoses suivants : antécédent de surdose, antécédent de trouble lié à l’utilisation de substances, doses d’opioïdes équivalentes à plus de 50 mg de morphine par jour ou utilisation concomitante de benzodiazépines (Dowell et al., 2016). Ceci est aussi recommandé par le National Opioid Use Guidelines Group (NOUGG) au Canada depuis 2017 (Busse et al., 2017). La naloxone peut donc être prescrite aux patients au département d’urgence, en clinique de dépendance et plus rarement en clinique de médecine familiale (Dunne, 2018). La sensibilisation au risque de surdose par la prescription de naloxone peut notamment diminuer les comportements à risque des patients (Behar et al., 2016). Aux États-Unis, une étude a démontré que les patients ayant reçu une prescription de naloxone de leur médecin diminuaient de 63,0 % leurs visites à l’urgence pour des symptômes reliés aux opioïdes dans l’année suivant l’intervention (Coffin et al., 2016). La prescription de naloxone aux patients à risque de surdose a généralement un haut taux d’acceptabilité auprès des patients et des prescripteurs, mais peut être difficile à implanter, car plusieurs professionnels de la santé manquent de temps et de connaissances pour éduquer leurs patients adéquatement (Behar et al., 2018 ; Binswanger et al., 2015 ; Peckham et al., 2018).
Prévention des surdoses en cliniques de médecine familiale : formations de groupe
La création de formations de groupe représente une alternative intéressante pour prévenir les surdoses chez les patients à risque en contexte médical de première ligne. Il est établi que les formations de groupe sont efficaces chez les patients souffrant de maladies chroniques comme le diabète : les patients apprennent les uns des autres et y trouvent une source importante de soutien (Bair, 2017). Certaines cliniques de première ligne spécialisées en troubles liés à l’usage des opioïdes ont commencé à offrir des formations aux patients sous TAO : les quelques études les décrivant ont rapporté une augmentation des connaissances à la suite de la formation et une proportion d’utilisation de la naloxone trois mois après la formation allant jusqu’à 13,0 % (Katzman et al., 2018 ; Lott et Rhodes, 2016 ; Walley et al., 2013). À notre connaissance, une seule étude a évalué une intervention de groupe chez les patients traités avec des opioïdes pour la douleur chronique (Spelman et al., 2017). À la suite d’une formation de 90 minutes en groupe de dix, tous les participants avaient apprécié l’expérience et avaient demandé une prescription de naloxone à leur médecin.
Comme professionnels oeuvrant en première ligne et fréquemment en contact avec des patients avec un trouble lié à l’usage des opioïdes, une réflexion s’impose quant au développement d’outils rejoignant la totalité de la population à risque de surdose. Ceci inclut les personnes consommatrices de substances psychoactives, mais aussi les patients sous TAO et les utilisateurs d’opioïdes pour le traitement de la douleur chronique. Au Québec, les groupes de médecine familiale représentent un contexte unique où des interventions de prévention des surdoses d’opioïdes peuvent être dispensées simultanément à des membres de ces trois groupes à risque. C’est dans cet esprit que nous nous sommes intéressés à l’évaluation d’une formation standardisée sur l’utilisation de naloxone afin de réduire les risques de surdose chez la population consommatrice d’opioïdes du GMF-U Charles-LeMoyne.
Modèle théorique
Le développement de la formation et du devis de recherche dont il est question dans cet article s’est inspiré du modèle logique théorique du changement de comportement (Brousselle et al., 2011 ; Mayne, 2017). Ce modèle suppose que les connaissances acquises lors d’une intervention augmentent les savoirs, les attitudes et les compétences. Par la suite, cette augmentation des capacités pourrait entraîner un changement de comportements. L’hypothèse émise est donc que la formation sur l’utilisation de la naloxone, en augmentant les connaissances quant aux surdoses, entraîne des changements de comportements qui pourraient subséquemment réduire le risque de surdose ou en améliorer la prise en charge.
Objectifs de l’étude
L’étude avait comme objectif primaire de déterminer la rétention des concepts clés en lien avec les facteurs de risque, la reconnaissance et la prise en charge d’une surdose aux opioïdes chez nos patients consommateurs d’opioïdes à la suite d’une formation sur l’utilisation de naloxone. En nous basant sur la littérature et le modèle théorique du changement de comportement, nous avons émis l’hypothèse qu’il y aurait une importante augmentation des connaissances à la suite de la formation et que celle-ci se maintiendrait dans le temps, de façon statistiquement significative.
Les objectifs secondaires étaient de déterminer la proportion de participants qui possèdent une trousse de naloxone sur eux lorsqu’ils consomment des opioïdes, la proportion de participants ayant été témoins d’une surdose d’opioïdes, la proportion d’utilisation de la naloxone par les participants au cours de la période de suivi ainsi que le niveau de confiance des participants acquis grâce à une formation de groupe.
Méthodologie
Contexte
Le Groupe de médecine familiale universitaire (GMF-U) Charles-LeMoyne est une clinique de médecine familiale située en Montérégie au Québec, qui traite une clientèle variée incluant 90 patients traités avec opioïdes pour la douleur chronique et 160 patients sous TAO pour un trouble lié à l’usage des opioïdes. La clinique regroupe 22 médecins de famille en plus d’être un centre de formation où des étudiants en médecine, médecins résidents, infirmières et infirmières praticiennes spécialisées sont formés annuellement.
Devis et recrutement
L’étude a été réalisée selon un devis de type quasi expérimental à simple insu. Le recrutement a été fait par un échantillonnage de convenance, avec une cible de 48 participants. De ces participants, un groupe de patients « douleur chronique » et un groupe de patients « TAO » ont été créés. Cette division en deux groupes permet de séparer une population ayant des troubles de consommation de substances psychoactives, d’une population qui n’a pas reçu ce diagnostic. Le GMF-U Charles-Lemoyne a donc été choisi comme lieu de recrutement par convenance, mais aussi, car la diversité de sa clientèle permettait de tester une intervention avec un public cible plus large.
La référence initiale vers l’équipe de recherche était basée sur le jugement du professionnel traitant qui, connaissant son patient depuis longtemps, identifiait s’il pouvait être intéressé par une formation sur la naloxone. Les participants potentiels devaient donc avoir été approchés par leur professionnel traitant et consenti à se faire contacter avant de recevoir un appel de la part de l’équipe de recherche. Des affiches de sollicitation ont aussi été installées dans la salle d’attente afin que les patients intéressés puissent en discuter directement avec leur professionnel traitant.
Les participants potentiels et éligibles ont ensuite été contactés par téléphone par l’équipe de recherche jusqu’à l’atteinte de l’échantillon désiré. Les critères d’inclusion pour participer à la formation étaient les suivants : être âgé de 18 ans et plus, comprendre le français écrit et parlé, être suivi dans un contexte médical de première ligne au GMF-U Charles-LeMoyne et avoir consommé des opioïdes au moins une fois par jour depuis trois mois (peu importe la dose) via une prescription pour la douleur chronique ou un TAO. Le seul critère d’exclusion était d’avoir préalablement reçu une formation de plus de cinq minutes sur l’utilisation de naloxone.
Intervention
L’intervention étudiée était la tenue d’une formation de 60 minutes, en groupes de maximum 12 personnes, au GMF-U Charles-LeMoyne. Cette dernière était dispensée par des membres de l’équipe de recherche et avait préalablement été élaborée par un médecin résident en santé publique et en médecine préventive.
Les cibles d’apprentissages incluaient : identifier les comportements augmentant le risque de surdose, reconnaître les signes et symptômes d’une surdose, intervenir en situation de surdose, administrer la naloxone par voie nasale ainsi qu’appeler les secours en cas de surdose.
De septembre 2018 à janvier 2019, trois formations ont eu lieu au GMF-U Charles-LeMoyne : deux formations pour le groupe « douleur chronique » et une formation pour le groupe « TAO ». À la fin de la formation, chaque patient recevait une trousse de naloxone par voie nasale. La formule de naloxone par voie nasale a été choisie, car il a été démontré qu’elle est préférée par les patients en comparaison avec la naloxone par injection (Ashrafioun et al., 2016 ; Dunn et al., 2018).
Considérations éthiques
Le protocole de recherche a préalablement été approuvé par le comité d’éthique du CSSS Montérégie-Centre. Avant de participer à la formation, les participants devaient également signer un formulaire de consentement. Un dédommagement financier de 15 $ pour s’être déplacé et un goûter ont aussi été offerts aux participants.
Instruments de mesure
Afin d’évaluer l’évolution des connaissances des participants dans le temps, nous avons choisi d’utiliser le questionnaire Opioid Overdose Knowledge Scale (OOKS), traduit en français, avec la permission de l’auteure, grâce à la procédure de l’OMS Management of substance abuse – Process of translation and adaptation of instruments, une procédure qui a comme but de créer un outil conceptuellement équivalent, en tenant compte de la réalité culturelle d’où il sera employé (WHO, 2010 ; Williams et al., 2013). Le questionnaire OOKS a été élaboré et validé afin d’évaluer les programmes de formation à l’utilisation de naloxone. Au niveau psychométrique, lors de l’étude de validation, le coefficient alpha (validité interne) était de 0,83 et le coefficient de corrélation intraclasse de 0,90 (Williams et al., 2013).
Les thèmes évalués par le questionnaire sont les facteurs de risque d’une surdose (par exemple prendre une dose d’opioïdes plus élevée que d’habitude), la reconnaissance de cette dernière (par exemple une respiration lente), les actions immédiates à entreprendre (par exemple appeler une ambulance), de même que les modalités d’administration de naloxone (par exemple la voie d’administration). Initialement utilisé pour des programmes chez des populations ayant des troubles de consommation de substances, il emploie le terme « héroïne », que nous avons substitué par le terme plus large « opioïde » par souci d’inclusion. Le pointage final est calculé sur un total de 44 points. Le questionnaire OOKS intégral est disponible en ligne au lien suivant : https://www.kcl.ac.uk/ioppn/depts/addictions/research/drugs/Naloxone/Resources. La version traduite est disponible pour le lecteur sur demande.
À notre connaissance, lors du début de notre étude, peu de questionnaires validés étaient disponibles pour évaluer les connaissances sur les surdoses d’opioïdes soit le OOKS, le Brief Opioid Overdose Knowledge questionnaire (BOOK) et le Brief Overdose Recognition and Response Assessment (BORRA). Le BOOK (Dunn et al., 2016) cible des milieux où la naloxone n’est pas encore disponible. Le BORRA (Green et al., 2008) ne couvre pas les notions concernant les facteurs de risque d’une surdose, les principes généraux de la prise en charge d’une surdose ou les effets de la naloxone. Ceci est la principale raison ayant mené Williams et son équipe à élaborer le questionnaire OOKS, qui couvre toutes ces notions. C’est d’ailleurs le questionnaire validé le plus utilisé dans les études visant à évaluer la performance des formations de prévention des surdoses d’opioïdes et c’est pour cette raison qu’il a été sélectionné pour cette étude (Franklin Edwards et al., 2020).
Un questionnaire colligeant des données démographiques sur les participants a aussi été distribué avant la formation (T0), tandis que le questionnaire administré trois mois post-formation (T2) était bonifié de quatre questions afin d’évaluer les objectifs secondaires. Les questions étaient les suivantes : « Avez-vous été témoin d’une surdose aux opiacés dans les trois derniers mois ? Depuis la formation, avez-vous eu à administrer des doses de naloxone ? Est-ce que votre naloxone est rapidement accessible lorsque vous consommez des opioïdes ou prenez votre prescription d’opioïdes ? Quel est votre niveau de confiance en votre capacité à utiliser votre naloxone en cas de surdoses ? »
Analyses statistiques
Les variables ont été étudiées en réalisant une série temporelle et en mesurant le pointage au questionnaire OOKS (variable dépendante continue). Les mesures ont été prises en trois temps (variables indépendantes catégorielles), soit au T0 avant la formation, au T1 immédiatement après la formation et au T2, soit trois mois après la formation. Les questionnaires ont été gérés par les membres de l’équipe ayant donné la formation.
À la suite d’un bilan initial, l’équipe a estimé à 250 personnes le nombre de participants potentiels à l’étude. Le nombre de participants ciblé pour atteindre une puissance statistique de 80,0 % était de 48. L’analyse statistique a été réalisée avec le modèle mixte linéaire SAS (généralisation ANOVA mesures répétées), un test qui tient compte des mesures relatives à un individu même si certaines données de la série temporelle sont absentes. Cette analyse permet aussi simultanément de détecter une différence entre les mesures d’OOKS répétées et une différence entre les deux groupes indépendants « TAO » et « douleur chronique ». Le logiciel utilisé était SAS® 9.4.
Résultats
Recrutement des participants
Au total, 23 participants ont participé aux formations après avoir été considérés comme éligibles : 17 dans le groupe « douleur chronique » et 6 dans le groupe « TAO ». Parmi les patients ayant initialement accepté de se faire contacter après avoir été sollicités par leur médecin de famille, dix-huit ont refusé de participer à la formation lorsque contactés par l’équipe de recherche. Les raisons évoquées pour le refus incluaient une faible perception de leur risque de surdose, un manque de temps ou un manque d’intérêt à faire partie d’un groupe. Nous n’avons pas pu récolter d’information concernant les patients ayant accepté de participer à la formation qui ne se sont finalement pas présentés. Respectivement, il y a eu une perte au suivi de trois individus dans le groupe « douleur chronique » et de deux individus dans le groupe « TAO » après la formation (T2), ce qui représente 17,6 % et 33,3 % de perte au suivi (figure 1).
Caractéristiques des participants
L’âge moyen des participants à l’étude était 58 ans et 60,9 % étaient des femmes. Pour ce qui est du niveau d’éducation, 50,1 % des participants « TAO » avaient un diplôme d’études secondaires et 41,2 % des participants « douleur chronique » avaient un diplôme d’études collégiales. À travers tous les participants, la consommation concomitante de benzodiazépines (34,8 %) et d’alcool (30,4 %) était présente (tableau 1).
Évolution des connaissances dans le temps
Au T0 (préformation), le groupe « TAO » avait un pointage OOKS de 31,8 (IC 95,0 %, 27,4-36,3 ; p<0,0001) et le groupe « douleur chronique » avait un pointage OOKS de 22,3 (IC 95,0 %, 19,7-24,9 ; p<0,0001) (tableau 2). La différence entre les deux groupes n’est plus statistiquement significative immédiatement après avoir assisté à la formation (T1).
Pour ce qui est de l’évolution des connaissances dans le temps, qui a été mesurée par le pointage moyen au questionnaire OOKS, les pointages des 23 participants inclus étaient de 24,8/44 (IC 95,0 %, 22,3-27,3 ; p<0,0001) à T0, 39,1/44 (IC 95,0 %, 36,6-41,6 ; p<0,0001) à T1 et 35,0/44 (IC 95,0 %, 32,3-37,7 ; p<0,0001) 3 mois après la formation (T2) (figure 2). Les résultats sont aussi statistiquement significatifs lorsqu’analysés par sous-groupes (tableau 2).
La puissance de l’étude, calculée a posteriori, s’élève à 95,9 % pour la différence de pointage entre les groupes et à 99,9 % pour la différence entre les trois temps de mesure, en considérant un risque alpha de 5,0 %.
Figure 1
Recrutement des participants
tableau 1
Caractéristiques démographiques des participants
Figure 2
Évolution des connaissances dans le temps
tableau 2
Pointage au questionnaire OOKS
Note. * Nombre initial de 23 participants ; perte de suivi au T2 pour 2 participants du groupe « TAO » et 3 du groupe « douleur chronique ».
Augmentation du niveau de confiance et utilisation de la naloxone après la formation
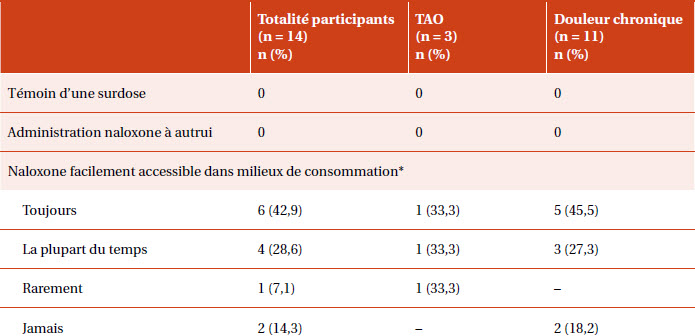
Pour ce qui est des objectifs secondaires (tableau 3), aucun des candidats n’a été témoin de surdose aux opioïdes ou n’a eu à administrer la naloxone durant la période de suivi de l’étude. La majorité des participants (71,4 %) avaient une trousse de naloxone facilement accessible lors de leur consommation d’opioïdes. Finalement, trois mois après leur formation (T2), 92,9 % des patients étaient confiants ou très confiants en leurs capacités à prendre en charge une surdose aux opioïdes s’ils en étaient témoins.
tableau 3
Utilisation de naloxone après la formation
Note. 9 abstentions de répondre pour ces questions : 3 dans le groupe « TAO » et 6 dans le groupe « douleur chronique ».
* 1 abstention de répondre additionnelle pour cette question dans le groupe « douleur chronique ».
Discussion
Les résultats décrits permettent de croire qu’une formation de groupe de 60 minutes a le potentiel d’augmenter de façon significative les connaissances et la confiance chez les patients que nous côtoyons en contexte médical de première ligne, que ce soit ceux traités avec opioïdes pour la douleur chronique ou ceux sous TAO. Cette augmentation des connaissances pourrait se maintenir trois mois après la formation. Nos résultats concordent avec les écrits antérieurs sur le sujet (Spelman et al., 2017). Il s’agit toutefois d’une des premières études à s’intéresser à l’efficacité d’une formation chez les patients traités pour la douleur chronique. Sous réserve d’être répétée à plus grande échelle dans des recherches futures, cette étude porte donc à croire que cette formation serait efficace chez les patients traités pour la douleur chronique.
Comme démontré dans le tableau 2, les patients sous opioïdes pour la douleur chronique ont généralement un niveau de connaissance moindre sur les risques et la gestion des surdoses, ce qui est compatible à la littérature existante sur cette question (Mueller et al., 2016 ; Nielsen et al., 2018). Ceci souligne l’importance de développer des interventions adaptées à cette catégorie de patients qu’on sait vulnérable.
En comparant les deux groupes ayant reçu la formation, nous observons une différence préformation (T0) entre le groupe « TAO » et le groupe « douleur chronique ». En effet, le groupe « TAO » possède de meilleures connaissances avant la formation (T0). Ceci est compatible avec la littérature existante qui démontre que les utilisateurs d’opioïdes illicites ont beaucoup de connaissances de base sur les surdoses (Behar et al., 2015). Cependant, les pointages immédiatement post-formation (T1), et trois mois après (T2), se nivellent par la suite. Ceci démontre que la formation, peu importe le niveau de connaissances de base, est efficace pour inculquer des connaissances, avec une moyenne de 35/44 au questionnaire OOKS, tous groupes confondus, trois mois après la formation.
Les échanges avec les participants permettent de croire qu’ils ont beaucoup apprécié leur expérience. Ils étaient curieux et posaient des questions aux formateurs. Plusieurs ont mentionné qu’ils auraient voulu inviter leurs proches à la formation. L’importance d’impliquer les proches a d’ailleurs été soulignée par une étude américaine, ciblant les patients traités avec méthadone, où la grande majorité des participants formés n’ont pas utilisé la naloxone sur eux-mêmes post-formation, mais plutôt sur un proche (Walley et al., 2013). Par ailleurs, nous croyons que séparer les participants « TAO » des participants « douleur chronique » améliore le niveau de confort des patients durant leur formation en plus de permettre des analyses par sous-groupe des résultats.
La durée du suivi (trois mois) était trop courte pour déterminer si les participants ont utilisé la naloxone à la suite de l’intervention. L’interprétation des objectifs secondaires (tableau 3) doit être faite prudemment étant donné le faible nombre de répondants, l’absence de prise de mesure avant la formation (T0) et le fait qu’aucun répondant n’ait été témoin de surdoses au cours du suivi. Il demeure intéressant de noter que la majorité des participants avaient une trousse de naloxone facilement accessible, la plupart du temps ou toujours, lors de leur consommation d’opioïdes trois mois post-formation. Le fait de fournir gratuitement une trousse de naloxone aux participants lors de la formation a possiblement contribué à ce résultat.
Une étude canadienne a démontré que les médecins de famille canadiens considèrent la prescription de naloxone et la formation de leurs patients à risque de surdose comme une intervention faisable et croient qu’une clinique médicale de première ligne est un endroit approprié pour l’implanter (Leece et al., 2015). Les éventuelles retombées positives nommées étaient l’amélioration de la relation patient-médecin, la diminution de la stigmatisation en lien avec la prise d’opioïdes et l’augmentation de l’accessibilité à la naloxone pour les patients traités pour la douleur chronique. Certaines barrières à l’implantation de cette intervention émergent toutefois de notre étude et elles sont concordantes avec la littérature.
Difficultés rencontrées et barrières à l’implantation
Tel qu’illustré dans la figure 1, le recrutement de participants pour la formation a été plus difficile que prévu. D’abord, la nature de notre protocole de recherche (limiter le recrutement aux patients initialement référés par leur professionnel traitant) a réduit le nombre de participants éligibles à 48. Une meilleure sensibilisation du personnel de la clinique aurait pu être faite pour augmenter le nombre de références. En effet, les dialogues médecin-patient concernant la prise d’opioïdes sont souvent délicats et la crainte du médecin d’offusquer son patient peut devenir une barrière à lui proposer une intervention visant à diminuer son risque de surdose (Binswanger et al., 2015). Alors qu’il est vrai que certains patients rapportent se sentir « jugés » par leur médecin concernant leur consommation d’opioïdes ou ont peur que leur médecin diminue leur prescription d’opioïdes s’ils utilisent la naloxone (Mueller et al., 2016), d’autres études démontrent plutôt que les patients ne seraient pas offensés de se faire offrir la naloxone et que ceci pourrait même améliorer leur lien de confiance avec leur médecin surtout quand la conversation est faite dans le respect (Kirane et al., 2016 ; Nielsen et al., 2018). Lors d’une étude en Californie, les patients traités pour la douleur chronique ont rapporté une augmentation de leur sentiment de sécurité après avoir reçu une prescription de naloxone (Behar et al., 2016).
Ensuite, plusieurs participants éligibles à notre étude ont refusé de participer à la formation ou ont été perdus au suivi. D’autres études ont aussi démontré que les patients traités avec opioïdes pour la douleur chronique sont particulièrement difficiles à rejoindre (Banjo et al., 2014 ; Spelman et al., 2017). Une faible conscience de leur risque, la crainte d’une dé-prescription de leur médication, le manque de temps ou la peur de la stigmatisation associée à la prise d’opioïdes exacerbée par une rencontre en groupe pourraient expliquer le faible taux de participation à la formation offerte. Certains patients pourraient préférer que la formation se fasse en privé lors d’un rendez-vous régulier avec leur médecin ; malheureusement, une telle approche a souvent été décrite comme difficile par les médecins en première ligne qui sont surchargés et manquent de temps (Peckham et al., 2018). Une étude qualitative descriptive conduite chez nos patients permettrait de mieux cerner ces barrières.
Finalement, certains professionnels de la santé craignent que la formation sur la naloxone auprès des patients à risque de surdose puisse entraîner un phénomène de compensations du risque, c’est-à-dire une augmentation de la consommation d’opioïdes post-formation (Binswanger et al., 2015). Dans une étude américaine en centre de désintoxication, 83,0 % des patients ont indiqué que leur consommation d’opioïdes augmenterait s’ils avaient accès à la naloxone par voie nasale (Kirane et al., 2016). Or, plusieurs études rapportent le contraire puisqu’à la suite d’une formation, les utilisateurs d’opioïdes comprennent mieux leur risque de surdose (Kerensky et Walley, 2017). L’orientation du Canada face à la crise des opioïdes étant la réduction des méfaits (Lancet, 2018), nous ne considérons pas que la crainte d’une compensation du risque devrait freiner l’implantation de formations sur la naloxone dans les cliniques de première ligne, mais ceci pourrait faire l’objet d’une étude subséquente.
Limites
L’étude décrite présente plusieurs limites. Tout d’abord, le nombre de participants (23) était grandement inférieur à ce qui était prévu (48) et il y a eu d’importantes pertes au suivi, malgré de multiples tentatives de rappeler les participants trois mois après le recrutement et des rappels deux jours avant les formations. Le fait que les deux groupes étaient de taille inégale, et qu’un des groupes ne comptait que six participants, rendait spéculative toute comparaison entre ceux-ci. De plus, il est difficile d’évaluer si la population ultimement étudiée était représentative de la population consommatrice d’opioïdes du GMF-U ou des cliniques de médecine familiale au Québec, car les données démographiques de celles-ci sont inconnues. Nous savons cependant que les décès pour suspicion d’intoxication aux opioïdes au Québec touchent davantage les hommes, alors que la population de notre étude était composée de femmes à 60,9 %. Bien que la puissance de l’étude demeure très haute étant donné la taille d’effet élevée, tous ces facteurs ont un impact sur la représentativité de notre échantillon et donc la validité externe de nos résultats.
Par ailleurs, le mode de recrutement de l’étude (participation volontaire, échantillonnage de convenance) a pu introduire un biais de volontariat. Il faut se demander si les participants étaient plus ouverts à se prêter à une formation que leurs pairs. Dans le même ordre d’idée, l’exclusion des participants qui ont été perdus au suivi a pu engendrer un biais de sélection. Ces biais auraient pu surestimer l’effet réel de l’intervention.
Pour ce qui est des objectifs secondaires, les questionnaires distribués à T2 concernant le niveau de confiance et l’accessibilité de la naloxone pendant la consommation d’opioïdes sont aussi sujets à d’importants biais de rappel et de désirabilité. En effet, les données recueillies étant de nature qualitative, les répondants ont pu surestimer leur niveau de confiance face à une surdose ou à quel point la naloxone avait été facile d’accès lors de leur consommation après la formation. Finalement, comme il a été mentionné plus haut, les objectifs secondaires n’ont malheureusement pas fait l’objet d’une collecte de données à T0 et aucune surdose n’a été observée au cours du suivi. Les résultats obtenus permettent donc d’émettre des hypothèses quant à certaines retombées positives possibles de l’intervention, mais nous ne pouvons conclure hors de tout doute à un lien causal entre notre intervention et ces résultats.
Bien que les résultats demeurent statistiquement significatifs, il serait judicieux de tester cette intervention avec un plus grand nombre de participants et d’ajouter une évaluation des objectifs secondaires à T0 avant de l’implanter à grande échelle. Un suivi des participants à plus long terme serait aussi pertinent, tout comme la validation d’un outil de mesure en français.
Conclusion
Alors que la majorité des interventions visant à diminuer la mortalité associée à la crise des opioïdes s’adresse aux populations ayant des troubles de consommation de substances, très peu d’initiatives se sont intéressées aux patients traités pour la douleur chronique ou sous TAO qui fréquentent les cliniques de médecine familiale. Cette clientèle ne fréquentant pas les ressources communautaires représente une fraction importante des hospitalisations et décès reliés aux surdoses ; c’est une population vieillissante qui souffre de multiples comorbidités la rendant particulièrement vulnérable face à l’intoxication. La prévention des surdoses en contexte médical de première ligne est donc une intervention primordiale.
Cette étude démontre le potentiel prometteur d’une formation de groupe sur la gestion des surdoses pour augmenter les connaissances et le niveau de confiance des patients en clinique de médecine familiale. Bien que l’étude ait été trop courte pour détecter un changement dans l’utilisation de la naloxone post-formation et aurait avantage à être répétée avec un plus large échantillon, les résultats permettent de faire un pas de plus vers la diversification des options et d’augmenter l’accessibilité de ce type d’activité de prévention à toutes les populations à risque de surdose. Notre étude souligne aussi l’importance pour les médecins de famille en première ligne de s’impliquer dans la prévention des effets néfastes des opioïdes chez leurs patients.
Nous croyons que ce projet pourrait également encourager le développement de ce type de stratégies à une plus grande échelle en première ligne. Intégrer de telles formations dans les centres de formation de futurs médecins (GMF-U au Québec) permettrait d’introduire les concepts de prévention et de réduction des méfaits en dépendance dans l’éducation médicale, en plus de sensibiliser les apprenants à l’importance de dépister les risques de surdose chez les patients vulnérables. Une telle intervention devrait cependant être intégrée à une approche globale de prévention des surdoses chez les patients traités chroniquement avec opioïdes, incluant aussi une attention à la surprescription et aux interactions médicamenteuses, des suivis rapprochés, un dépistage du mésusage, ainsi qu’une réévaluation fréquente des doses (Coe et Walsh, 2015). À l’avenir, il est probable que l’intervention puisse être dispensée par des professionnels de la santé autres que médecins, comme c’est déjà le cas pour plusieurs interventions de prévention en première ligne. Finalement, il serait intéressant d’évaluer l’intérêt des membres de la famille des consommateurs chroniques d’opioïdes à suivre eux-mêmes ces types de formation, afin qu’ils soient mieux sensibilisés et prêts à intervenir en cas de surdose chez leurs proches.
Parties annexes
Remerciements
Nous tenons à chaudement remercier Isabelle Gendron (B. Sc. Inf) et Annie Rouleau (B. Sc. Inf.), infirmières cliniciennes au GMF-U Charles-LeMoyne et au Centre de réadaptation en dépendance (CRD) Le Virage, pour leur précieuse collaboration tout au long du projet ainsi que Dr Guillaume Vandal (MD) pour avoir mis sur pied la formation offerte aux participants. Cet article est dédié à la mémoire du Dr Huy Hao Do.
Bibliographie
- Adewumi, A. D., Hollingworth, S. A., Maravilla, J. C., Connor, J. P. et Alati, R. (2018). Prescribed Dose of Opioids and Overdose: A Systematic Review and Meta-Analysis of Unintentional Prescription Opioid Overdose. CNS Drugs, 32(2), 101-116. https://doi.org/10.1007/s40263-018-0499-3
- Agence de la santé publique du Canada. (2020). Méfaits associés aux opioïdes au Canada – Infobase de la santé publique. https://sante-infobase.canada.ca/mefaits-associes-aux-substances/opioides/
- Ashrafioun, L., Gamble, S., Herrmann, M. et Baciewicz, G. (2016). Evaluation of knowledge and confidence following opioid overdose prevention training: A comparison of types of training participants and naloxone administration methods. Substance Abuse, 37(1), 76-81. https://doi.org/10.1080/08897077.2015.1110550
- Atrid Brousselle, F., Champagne, A.-P. et Contandriopoulos, Z. H. (2011). L’évaluation : concepts et méthodes (2e éd.). Les Presses de l’Université de Montréal. https://www.pum.umontreal.ca/catalogue/levaluation-concepts-et-methodes-2e-edition
- Bair, M. J. (2017). Using Group Visits to Provide Overdose Education and Distribute Naloxone to High-Risk Primary Care Patients. Pain Medicine, 18, 2263-2265. https://doi.org/10.1093/pm/pnx279
- Banjo, O., Tzemis, D., Al-Qutub, D., Amlani, A., Kesselring, S. et Buxton, J. A. (2014). A quantitative and qualitative evaluation of the British Columbia Take Home Naloxone program. CMAJ Open, 2(3), E153-E161. https://doi.org/10.9778/cmajo.20140008
- Behar, E., Bagnulo, R. et Coffin, P. O. (2018). Acceptability and feasibility of naloxone prescribing in primary care settings: A systematic review. Preventive Medicine, 114, 79-87. https://doi.org/10.1016/j.ypmed.2018.06.005
- Behar, E., Rowe, C., Santos, G. M., Murphy, S. et Coffin, P. O. (2016). Primary care patient experience with naloxone prescription. Annals of Family Medicine, 14(5), 431-436. https://doi.org/10.1370/afm.1972
- Behar, E., Santos, G. M., Wheeler, E., Rowe, C. et Coffin, P. O. (2015). Brief overdose education is sufficient for naloxone distribution to opioid users. Drug and Alcohol Dependence, 148, 209-212. https://doi.org/10.1016/j.drugalcdep.2014.12.009
- Binswanger, I. A., Koester, S., Mueller, S. R., Gardner, E. M., Goddard, K. et Glanz, J. M. (2015). Overdose Education and Naloxone for Patients Prescribed Opioids in Primary Care: A Qualitative Study of Primary Care Staff. Journal of General Internal Medicine, 30(12), 1837-1844. https://doi.org/10.1007/s11606-015-3394-3
- Brousselle, A., Champagne, A., Contandriopoulos, A.-P. et Hartz, Z. (2011). L’évaluation : concepts et méthodes (2e éd.). Les Presses de l’Université de Montréal.
- Busse, J., Busse, J. W., Guyatt, G. H., Carrasco, A., Akl, E. et Tugwell, P. (2017). The 2017 Canadian Guideline for Opioids for Chronic Non-Cancer Pain. National Opioid Use Guidelines Group.
- Carter, C. I. et Graham, B. (2013). Opioid overdose prevention & response in canada. Canadian Drug Policy Coalition. https://drugpolicy.ca/wp-content/uploads/2013/01/CDPC_OverdosePreventionPolicy_Final_July2014.pdf
- Clark, A. K., Wilder, C. M. et Winstanley, E. L. (2014). A systematic review of community opioid overdose prevention and naloxone distribution programs. Journal of Addiction Medicine, 8(3), 153-163. https://doi.org/10.1097/ADM.0000000000000034
- Coe, M. A. et Walsh, S. L. (2015). Distribution of naloxone for overdose prevention to chronic pain patients. Preventive Medicine, 80, 41-43. https://doi.org/10.1016/j.ypmed.2015.05.016
- Coffin, P. O., Behar, E., Rowe, C., Santos, G.-M., Coffa, D., Bald, M. et Vittinghoff, E. (2016). Non-randomized intervention study of naloxone co-prescription for primary care patients on long-term opioid therapy for pain. Annals Internal Medicine, 165(4), 245-252. https://doi.org/10.7326/M15-2771
- Dietze, P. M., Draper, B., Olsen, A., Chronister, K. J., van Beek, I., Lintzeris, N., Dwyer, R., Nelson, M. et Lenton, S. (2018). Does training people to administer take-home naloxone increase their knowledge? Evidence from Australian programs. Drug and Alcohol Review, 37(4), 472-479. https://doi.org/10.1111/dar.12680
- Direction de la santé publique de la Montérégie. (2020). Portrait des surdoses aux opioïdes.
- Dowell, D., Haegerich, T. M. et Chou, R. (2016). CDC guideline for prescribing opioids for chronic pain-United States, 2016. Journal of the American Medical Association, 315(15), 1624-1645. https://doi.org/10.1001/jama.2016.1464
- Dunn, K. E., Barrett, F. S. et Bigelow, G. E. (2018). Naloxone Formulation For Overdose Reversal Preference Among Patients Receiving Opioids for Pain Management. Addictive Behaviors, 86, 56-60. https://doi.org/10.1016/j.addbeh.2018.03.011
- Dunn, K. E., Barrett, F. S., Fingerhood, M. et Bigelow, G. E. (2017). Opioid Overdose History, Risk Behaviors, and Knowledge in Patients Taking Prescribed Opioids for Chronic Pain. Pain Medicine, 18, 1505-1515. https://doi.org/10.1093/pm/pnw228
- Dunn, K. E., Barrett, F. S., Yepez-Laubach, C., Meyer, A. C., Hruska, B. J., Sigmon, S. C., Fingerhood, M. et Bigelow, G. E. (2016). Brief opioid overdose knowledge (BOOK): A questionnaire to assess overdose knowledge in individuals who use illicit or prescribed opioids. Journal of Addiction Medicine, 10(5), 314-323. https://doi.org/10.1097/ADM.0000000000000235
- Dunn, K. M., Saunders, K. W., Rutter, C. M., Banta-Green, C. J., Merrill, J. O., Sullivan, M. D., Weisner, C. M., Silverberg, M. J., Campbell, C. I., Pasty, B. M. et Von Korff, M. (2010). Opioid prescriptions for chronic pain and overdose: A cohort study. Annals of Internal Medicine, 152(2), 85-92. https://doi.org/10.7326/0003-4819-152-2-201001190-00006
- Dunne, R. B. (2018). Prescribing naloxone for opioid overdose intervention. Pain Management, 8(3), 197-208. https://doi.org/10.2217/pmt-2017-0065
- Enteen, L., Bauer, J., Mclean, R., Wheeler, E., Huriaux, E., Kral, A. H. et Bamberger, J. D. (2010). Overdose Prevention and Naloxone Prescription for Opioid Users in San Francisco. Journal of Urban Health: Bulletin of the New York Academy of Medicine, 87(6), 931-941. https://doi.org/10.1007/s11524-010-9495-8
- Franklin Edwards, G., Mierisch, C., Mutcheson, B., Horn, K. et Henrickson Parker, S. (2020). A review of performance assessment tools for rescuer response in opioid overdose simulations and training programs. Preventive Medicine Reports, 20, 1-18. https://doi.org/10.1016/j.pmedr.2020.101232
- Green, T. C., Heimer, R. et Grau, L. E. (2008). Distinguishing signs of opioid overdose and indication for naloxone: an evaluation of six overdose training and naloxone distribution programs in the United States. Addiction, 103(6), 979-989. https://doi.org/10.1111/j.1360-0443.2008.02182.x
- Institut national d’excellence en santé et services sociaux. (2018). Naloxone. https://www.inesss.qc.ca/thematiques/medicaments/protocoles-medicaux-nationaux-et-ordonnances-associees/naloxone.html
- Institut national de santé publique du Québec. (2017). Crise d’opioïdes au Canada : les gouvernements passent à l’action. https://www.inspq.qc.ca/es/node/10171
- Institut national de santé publique du Québec. (2021). Surdoses d’opioïdes. https://www.inspq.qc.ca/substances-psychoactives/opioides/surdoses
- Irvine, M. A., Kuo, M., Buxton, J. A., Balshaw, R., Otterstatter, M., Macdougall, L., Milloy, M.-J., Bharmal, A., Henry, B., Tyndall, M., Coombs, D. et Gilbert, M. (2019). Modelling the combined impact of interventions in averting deaths during a synthetic-opioid overdose epidemic. Addiction, 114(9), 1602-1613. https://doi.org/10.1111/add.14664
- Ives, T. J., Chelminski, P. R., Hammett-Stabler, C. A., Malone, R. M., Perhac, J. S., Potisek, N. M., Shilliday, B. B., DeWalt, D. A. et Pignone, M. P. (2006). Predictors of opioid misuse in patients with chronic pain: A prospective cohort study. BMC Health Services Research, 6, 1-10. https://doi.org/10.1186/1472-6963-6-46
- Katzman, J. G., Takeda, M. Y., Bhatt, S. R., Balasch, M. M., Greenberg, N. et Yonas, H. (2018). An Innovative Model for Naloxone Use Within an OTP Setting: A Prospective Cohort Study. Journal of Addictive Medicine, 12(2), 113-118. https://doi.org/10.1097/ADM.0000000000000374
- Kerensky, T. et Walley, A. Y. (2017). Opioid overdose prevention and naloxone rescue kits: what we know and what we don’t know. Addiction Science & Clinical Practice, 12(4), 1-7. https://doi.org/10.1186/s13722-016-0068-3
- Kirane, H., Ketteringham, M., Bereket, S., Dima, R., Basta, A., Mendoza, S. et Hansen, H. (2016). Awareness and Attitudes Toward Intranasal Naloxone Rescue for Opioid Overdose Prevention. Journal of Substance Abuse Treatment, 69, 44-49. https://doi.org/10.1016/j.jsat.2016.07.005
- Lancet, T. (2018). A public health approach to Canada’s opioid crisis. The Lancet Public Health, 3, e204. https://doi.org/10.1016/S2468-2667(18)30078-1
- Leece, P., Orkin, A., Ccfp, M., Shahin, R. et Steele, L. S. (2015). Can naloxone prescription and overdose training for opioid users work in family practice? Perspectives of family physicians. Canadian Family Physician, 61, 538-543.
- Lopez Gaston, R., Best, D., Manning, V. et Day, E. (2009). Can we prevent drug related deaths by training opioid users to recognise and manage overdoses? Harm Reduction Journal, 6(26), 1-8. https://doi.org/10.1186/1477-7517-6-26
- Lott, D. C. et Rhodes, J. (2016). Opioid overdose and naloxone education in a substance use disorder treatment program. American Journal on Addictions, 25(3), 221-226. https://doi.org/10.1111/ajad.12364
- Mayne, J. (2017). Théories du changement: Comment élaborer des modèles utiles. Canadian Journal of Program Evaluation, 32(2), 174-201. https://doi.org/10.3138/cjpe.31144
- Mcdonald, R. et Strang, J. (2016). Are take-home naloxone programmes effective? Systematic review utilizing application of the Bradford Hill criteria. Addiction, 111, 1177-1187. https://doi.org/10.1111/add.13326
- Méta d’Âme. (2020). Programme PROFAN, formation sur la Naloxone. http://metadame.org/profan-formation-naloxone/
- Mueller, S. R., Koester, S., Glanz, J. M., Gardner, E. M. et Binswanger, I. A. (2016). Attitudes Toward Naloxone Prescribing in Clinical Settings: A Qualitative Study of Patients Prescribed High Dose Opioids for Chronic Non-Cancer Pain. Journal of General Internal Medicine, 32(3), 277-283. https://doi.org/10.1007/s11606-016-3895-8
- Mueller, S. R., Walley, A. Y., Calcaterra, S. L., Glanz, J. M. et Binswanger, I. A. (2015). A Review of Opioid Overdose Prevention and Naloxone Prescribing: Implications for Translating Community Programming into Clinical Practice. Substance Abuse, 36(2), 240-253. https://doi.org/10.1080/08897077.2015.1010032
- Nielsen, S., Peacock, A., Lintzeris, N., Bruno, R., Larance, B. et Degenhardt, L. (2018). Knowledge of Opioid Overdose and Attitudes to Supply of Take-Home Naloxone Among People with Chronic Noncancer Pain Prescribed Opioids. Pain Medicine, 19, 533-540. https://doi.org/10.1093/pm/pnx021
- Peckham, A. M., Niculete, M. E., Steinberg, H. et Boggs, D. L. (2018). A Survey of Prescribers’ Attitudes, Knowledge, Comfort, and Fear of Consequences Related to an Opioid Overdose Education and Naloxone Distribution Program. Journal of Public Health Management and Practice, 24(4), 310-317. https://doi.org/10.1097/PHH.0000000000000668
- Santé Canada. (2017). Enquête canadienne sur le tabac, l’alcool et les drogues (ECTAD) : sommaire des résultats pour 2017.https://www.canada.ca/fr/sante-canada/services/enquete-canadienne-tabac-alcool-et-drogues/sommaire-2017.html
- Seal, K. H., Thawley, R., Gee, L., Bamberger, J., Kral, A. H., Ciccarone, D., Downing, M. et Edlin, B. R. (2005). Naloxone Distribution and Cardiopulmonary Resuscitation Training for Injection Drug Users to Prevent Heroin Overdose Death: A Pilot Intervention Study. Journal of Urban Health: Bulletin of the New York Academy of Medicine, 82(2), 303-311. https://doi.org/10.1093/jurban/jti053
- Spelman, J. F., Peglow, S., Schwartz, A. R., Burgo-Black, L., Mcnamara, K. et Becker, W. C. (2017). Group Visits for Overdose Education and Naloxone Distribution in Primary Care: A Pilot Quality Improvement Initiative. Pain Medicine, 18, 2325-2330. https://doi.org/10.1093/pm/pnx243
- Strang, J., Bird, S. M., Dietze, P., Gerra, G. et McLellan, A. T. (2014). Take-home emergency naloxone to prevent deaths from heroin overdose: Time to save lives. British Medical Journal, 349, 1-2. https://doi.org/10.1136/bmj.g6580
- Strang, J., Manning, V., Mayet, S., Best, D., Titherington, E., Santana, L., Offor, E. et Semmler, C. (2008). Overdose training and take-home naloxone for opiate users: Prospective cohort study of impact on knowledge and attitudes and subsequent management of overdoses. Addiction, 103(10), 1648-1657. https://doi.org/10.1111/j.1360-0443.2008.02314.x
- Strang, J., Mcdonald, R., Campbell, G., Degenhardt, L., Nielsen, S., Ritter, A. et Dale, O. (2019). Take-Home Naloxone for the Emergency Interim Management of Opioid Overdose: The Public Health Application of an Emergency Medicine. Drugs, 79, 1395-1418. https://doi.org/10.1007/s40265-019-01154-5
- Tobin, K. E., Sherman, S. G., Beilenson, P., Welsh, C. et Latkin, C. A. (2009). Evaluation of the Staying Alive programme: Training injection drug users to properly administer naloxone and save lives. International Journal of Drug Policy, 20, 131-136. https://doi.org/10.1016/j.drugpo.2008.03.002
- Wagner, K. D., Valente, T. W., Casanova, M., Partovi, S. M., Mendenhall, B. M., Hundley, J. H., Gonzalez, M. et Unger, J. B. (2010). Evaluation of an Overdose Prevention and Response Training Programme for Injection Drug Users in the Skid Row Area of Los Angeles, California. International Journal of Drug Policy, 21(3), 186-193. https://doi.org/10.1016/j.drugpo.2009.01.003
- Walley, A. Y., Doe-Simkins, M., Quinn, E., Pierce, C., Xuan, Z. et Ozonoff, A. (2013). Opioid overdose prevention with intranasal naloxone among people who take methadone. Journal of Substance Abuse Treatment, 44, 241-247. https://doi.org/10.1016/j.jsat.2012.07.004
- World Health Organization. (2010). Process of translation and adaptation of instruments. https://www.who.int/substance_abuse/research_tools/translation/en/
- World Health Organization. (2018). Information sheet on opioid overdose. Dans WHO Key Facts. World Health Organization.
- Williams, A. V., Strang, J. et Marsden, J. (2013). Development of Opioid Overdose Knowledge (OOKS) and Attitudes (OOAS) Scales for take-home naloxone training evaluation. Drug and Alcohol Dependence, 132, 383-386. https://doi.org/10.1016/j.drugalcdep.2013.02.007
Liste des figures
Figure 1
Recrutement des participants
Figure 2
Évolution des connaissances dans le temps
Liste des tableaux
tableau 1
Caractéristiques démographiques des participants
tableau 2
Pointage au questionnaire OOKS
tableau 3
Utilisation de naloxone après la formation