Résumés
Résumé
Ce travail a porté sur la déstabilisation d’une émulsion d’huile de coupe algérienne (Tasfalout 22/B) par électrocoagulation (EC) en batch en utilisant des électrodes de fer. L’efficacité du procédé est évaluée par la mesure de la turbidité. Une meilleure efficacité de déstabilisation est obtenue par une augmentation de la densité de courant de 50 à 350 A•m‑2 pour un temps d’électrolyse de 15 min et des concentrations en huile de coupe de 1 % (p/p), 2 % (p/p) et 4 %(p/p). Un rendement d’élimination en turbidité de 99 % a été obtenu pour une émulsion à 4 % (p/p), une densité de courant de 150 A•m‑2 et un temps d’électrolyse de 120 min.
Le suivi de la cinétique de dissolution de l’électrode de fer sur une période de 120 minutes a montré qu’une même efficacité du procédé peut être obtenue par une diminution du temps d’électrolyse et une augmentation de la densité de courant.
Une étude comparative des performances de l’électrocoagulation et de la coagulation-floculation au chlorure ferrique hydraté (FeCl3•6H2O), vis-à-vis de la déstabilisation d’une émulsion d’huile de coupe, a été réalisée. Elle a mis en évidence l’avantage de la coagulation-floculation pour l’émulsion à 1 % (p/p), pour les différentes densités de courant testées en électrocoagulation. Par contre, les rendements d’élimination pour les deux procédés sont sensiblement similaires pour les émulsions plus concentrées (2 % (p/p) et 4 % (p/p)), pour une densité de courant de 150 A•m‑2. Le pH des émulsions obtenu par les deux procédés après le traitement est différent. Le milieu reste alcalin dans l’électrocoagulation et il devient acide dans la coagulation floculation.
Mots clés:
- électrocoagulation,
- émulsion (huile/eau),
- huile de coupe,
- électrodes de fer,
- déstabilisation,
- turbidité,
- coagulation-floculation,
- électrolyse
Abstract
This work focuses on the breakdown of an Algerian cutting oil emulsion (Tasfalout 22/B) by batch electrocoagulation (EC) using iron electrodes. The efficiency of the process was estimated from turbidity measurements. An improved efficiency of destabilization was obtained by increasing the current density from 50 to 350 A•m‑2, over an electrolysis time of 15 min and using cutting oil concentrations of 1% (w/w), 2% (w/w) and 4% (w/w). Monitoring of the kinetics of the electrode dissolution over a period of 120 min showed that a similar process efficiency was obtained by decreasing the electrolysis time and by increasing the current density. A 99% removal of turbidity was obtained for an emulsion of 4% (w/w) with a current density of 150 A•m‑2 and an electrolysis time of 120 min.
A comparison of the performances of electrocoagulation and of coagulation-flocculation with hydrated ferric chloride (FeCl3•6H2O) processes was carried out, with respect to the destabilization of cutting oil emulsion. This comparison highlighted the advantage of the coagulation-flocculation process for the of 1% (w/w) emulsion at different electrocoagulation current densities. However, for a current density of 150 A•m‑2, the removal efficiency of both processes was similar for the emulsion with higher cutting oil concentrations (2% (w/w) and 4% (w/w)). The pH of the emulsion obtained by the two processes following treatment varied. The medium remained alkaline during the electrocoagulation process and became acidic during the coagulation-flocculation process.
Keys-words:
- electrocoagulation,
- emulsion (oil/water),
- cutting oil,
- iron electrodes,
- destabilization,
- turbidity,
- coagulation-flocculation,
- electrolysis
Corps de l’article
1. Introduction
L’électrocoagulation est une méthode simple et efficace pour le traitement des eaux usées, en particulier celles contaminées par les composants organiques et huileux. Cette technique entraîne une dissolution du métal de l’anode avec formation simultanée d’ions hydroxyles et de gaz hydrogène à la cathode. Elle a été proposée avant le début du XXe siècle, dans une usine d’épuration à Londres construite en 1889 en vue de l’épuration des eaux d’égout mélangées à l’eau de mer.
En 1909, aux Etats-Unis, J.T Harries déposa un brevet d’épuration des eaux usées par électrolyse avec anodes sacrificatoires en aluminium et en fer (VIK et al., 1984). Dans les années 1940, un appareil a été réalisé, appelé le « coagulateur électronique » dont le principe est de dissoudre électrochimiquement l’aluminium constituant l’anode, celui-ci réagit en solution avec l’ion hydroxyde issu de la cathode pour former in situ l’hydroxyde d’aluminium. L’hydroxyde flocule et coagule les solides en suspension purifiant ainsi l’eau (MATTESON et al., 1995).
Un dispositif similaire a été employé en Grande-Bretagne en 1956 utilisant des électrodes de fer pour traiter une eau de rivière. Pendant une vingtaine d’années, le procédé d’électrocoagulation a été peu développé du fait du coût élevé des investissements et de la mauvaise connaissance de ses avantages. Il a été principalement concurrencé par les procédés de traitement chimique, sans pour cela avoir été totalement écarté. Il a commencé à se développer avec les progrès des procédés électrochimiques et la réglementation sur les rejets de plus en plus stricte.
Ce nouvel essor de l’électrocoagulation est en partie dû à la relative diminution des coûts d’investissement et d’exploitation et aussi au large spectre de polluants pouvant être éliminés. En effet, l’électrocoagulation a la capacité d’éliminer une large gamme de polluants allant de : métaux lourds (OSIPENKO et al.,1977); produits pétroliers (AMOSOV et al., 1976); couleurs à partir de solutions contenant des colorants (DO et CHEN, 1994); fluor (MAMERI et al., 1998); solides en suspension (MATTESON et al., 1995); humus aquatiques (VIK et al., 1984) et de lixiviats stabilisés (LABANOWSKI et al., 2006). Plusieurs autres applications de l’électrocoagulation sont présentées dans la bibliographie. Ces travaux de recherche ont utilisé l’aluminium ou le fer comme électrodes consommables. Plusieurs conditions opératoires telles que concentrations du dépolluant, acidité du milieu aqueux, densités de courant et temps de traitement, ont été testées. Ces études ont montré que ce procédé est satisfaisant pour la plupart des effluents. Comme tout procédé de traitement des eaux, l’efficacité est très influencée par les variations de la charge polluante.
Le matériau constituant les électrodes influence visiblement la performance du réacteur d’électrocoagulation. Il détermine la nature du cation introduit en solution. Plusieurs chercheurs ont étudié l’incidence du matériau de l’électrode avec diverses théories. Les plus communes des électrodes sont des plaques d’aluminium ou de fer, en raison de leur faible coût, de leur disponibilité et de leur efficacité (NOVIKOVA et al., 1982; PICARD et al., 2000; VIK et al., 1984). Un groupe de chercheurs a examiné la relation entre la « taille » du cation introduit et l’efficacité d’élimination de matières organiques. La taille du cation produit (10-30 µm pour Fe3+ comparé avec 0,05-1 µm pour Al3+) suggère une efficacité plus élevée pour les électrodes de fer. Leur conclusion est basée sur une seule expérience, utilisant la demande chimique en oxygène (DCO) comme paramètre de mesure de l’efficacité (BAKLAN et KOLESNIKOVA, 1996).
Il a été observé que l’électrocoagulation est fortement améliorée avec des électrodes en aluminium en comparaison avec l’acier. Ceci est attribué à l’efficacité plus élevée due à la formation in situ de complexes d’hydroxydes d’aluminium par hydrolyse de l’ion aluminate, qui ne se présente pas avec des électrodes en acier (HULSER et al., 1996).
Une étude comparative a été faite sur la performance des électrodes de fer et d’aluminium pour éliminer la couleur contenue dans des solutions (DO et CHEN, 1994). La conclusion de leurs travaux est que les conditions optimales d’électrocoagulation varient avec le choix des électrodes (fer ou aluminium), dépendant aussi des paramètres suivants :
la concentration initiale du polluant;
la nature du polluant;
la vitesse d’agitation;
et l’intensité.
L’une des limitations de l’électrocoagulation est la passivation des électrodes. Cette passivation (formation d’une couche protectrice à la surface) des électrodes est en rapport direct avec la longévité du processus. La passivation des électrodes d’aluminium a été largement observée dans la littérature (NIKOLAEV et al., 1982; NOVIKOVA et al., 1982; OSIPENKO et POGORELYI, 1977).
Il a été observé également que durant l’électrocoagulation avec des électrodes de fer, des dépôts de carbonate de calcium et d’hydroxyde de magnésium étaient formés à la cathode et une couche d’oxyde formée à l’anode.
Diverses méthodes de prévention et/ou de contrôle de passivation des électrodes ont été examinées, parmi lesquelles on citera :
changement de polarité des électrodes;
introduction d’agents inhibiteurs;
nettoyage mécanique des électrodes.
Selon ces chercheurs, la plus rentable et la plus fiable méthode de maintenance des électrodes est le nettoyage mécanique des électrodes (NIKOLAEV et al., 1982).
L’électrocoagulation se caractérise par une génération d’ions métalliques (Fe2+ ou Al3+) due à l’oxydation de l’anode (équations 1 et 5). Les ions métalliques réagissent à leur tour avec les ions hydroxyles (OH-) produits à la cathode avec un dégagement d’hydrogène (H2) (équations 3 et 7). Les matières en suspension interagissent avec les bulles de gaz pour former des flocs qui seront ensuite concentrés, collectés et éliminés. Ce processus contribue aussi à une coagulation par neutralisation des particules colloïdales chargées négativement. À titre d’exemple, l’oxydation du fer dans le système électrolytique produit l’hydroxyde de fer (Fe (OH)n) où n est égal à 2 ou à 3 (équations 2 et 6).
Deux mécanismes ont été proposés pour expliquer la formation de Fe (OH)n (DANESHVAR et al., 2003; LARUE et al., 2002; MOLLAH et al., 2001) :
• Premier mécanisme
Anode :
Cathode :
Global :
• Deuxième mécanisme :
Anode :
Cathode :
Global :
L’hydrogène ainsi généré participe donc à la flottation des flocs et favorise ainsi tant l’élimination des matières en suspension que l’élimination des composés organiques dissous adsorbés partiellement sur les flocs.
Les hydroxydes de fer (Fe (OH)n(s)) restent dans la solution aqueuse sous forme d’une suspension gélatineuse, pouvant éliminer les polluants de l’eau usée (IBANEZ et al., 1998; XINHUA XU et XIANGFENG ZHU, 2004) soit par :
complexation de surface : le polluant est comme un ligand (L) qui se fixe chimiquement à l’ion hydraté Fe (OH)n
Attraction électrostatique : les particules d’oxydes de fer hydratées possèdent des zones chargées positivement et négativement, qui vont attirer les charges opposées des polluants, et les éliminer de la solution par décantation.
Cependant, en examinant le diagramme de Pourbaix (diagramme Eh-pH) (POURBAIX, 1974), celui-ci montre que l’ion Fe3+ est stable seulement dans un milieu acide très oxydant, par contre l’ion Fe2+ est stable dans un intervalle Eh‑pH relativement large. Le composé insoluble Fe (OH)3 est l’espèce prédominante en fer dans un large intervalle Eh-pH.
Généralement, il est noté que les complexes de types hydroxydes sont formés après oxydation initiale du fer à l’anode selon les réactions données précédemment (équations 5 et 6).
Dans un environnement anaérobie non oxydant, et à un pH suffisamment élevé, l’hydroxyde ferreux précipitera selon la réaction (équation 6).
De même, la dissociation des molécules d’eau à l’anode génère une concentration élevée en protons selon la réaction :
Par contre, en solution en milieu oxygéné et à faible pH, les ions Fe2+ s’oxydent en ions Fe3+ , selon la réaction :
Les ions Fe3+ subiront une hydratation, la forme du modèle dépendra du pH. En milieu acide, les réactions suivantes ont été proposées (XINHUA XU et XIANGFENG ZHU, 2004) :
D’autres formes hydratées de l’ion Fe3+, dépendant du pH, ont été suggérées (KOBYA et al., 2003) : Fe(H2O)23+, Fe(H2O)5OH2+, Fe(OH)2+, Fe(OH)2+, Fe2(OH)24+, Fe(OH)4-, Fe(OH)63‑, Fe(H2O)4(OH)2+, Fe2(H2O)8(OH)24+ et Fe2(H2O)6(OH)42+.
Ces complexes jouent le rôle de coagulant. Ils s’adsorbent sur les particules, et annulent ainsi les charges colloïdales, ce qui conduit à la déstabilisation des émulsions stabilisées par des agents tensioactifs (cas des huiles de coupe). Ce rôle est similaire à celui des coagulants chimiques dans les traitements classiques de coagulation.
L’objectif de cette étude est de déstabiliser une émulsion d’huile de coupe algérienne (Tasfalout/22B) par électrocoagulation et par coagulation-floculation et de comparer ces deux procédés.
2. Matériels et méthodes
Le dispositif expérimental d’électrocoagulation est composé de deux électrodes de fer (acier ordinaire) de mêmes dimensions (198 mm × 48 mm) plongées dans un bécher de 1 litre. Le volume des émulsions traitées est de 900 mL. La surface immergée de chaque électrode est de 69,6 cm2 et la distance les séparant est de 2 cm. Ces deux paramètres seront maintenus constants durant toutes les expérimentations. Ces électrodes sont branchées aux bornes d’une alimentation en courant continu (générateur) dont la tension maximale est de 26 V et l’intensité de courant maximale de 12 A. La tension et l’intensité de courant sont mesurées respectivement à l’aide d’un voltmètre et d’un ampèremètre. Les appareils électriques utilisés sont de marque PHYWE.
L’échantillonnage est réalisé en cours de manipulation à l’aide d’une seringue dans la zone clarifiée de l’émulsion d’huile de coupe. Le volume des échantillons est de 25 mL. Avant d’effectuer les analyses, ces échantillons sont filtrés sur un équipement de filtration sous vide afin d’éliminer les flocs non décantés. Les filtres utilisés ont un seuil de filtration de 16 microns (grade 12).
Les essais de coagulation-floculation ont été réalisés sur un jar-test, composé d’une série d’agitateurs à pales, au nombre de quatre montés sur un banc lumineux. La vitesse des pales est réglable et identique d’un agitateur à l’autre. Les essais ont été réalisés dans des béchers de 1 litre. Le volume des émulsions traitées était de 900 mL.
Lors de l’ajout du coagulant, la vitesse d’agitation est réglée à 180 t•min‑1 pendant 1 minute. Cette vitesse est ensuite réduite à 40 t•min‑1 pendant 14 minutes jusqu’à la prise de l’échantillon.
Le volume des échantillons est de 25 mL. Ces échantillons sont filtrés sur un équipement de filtration sous vide. Les conditions opératoires de la coagulation-floculation (concentrations des émulsions, volume, temps de traitement etc.) sont identiques à celles utilisées dans le cas du traitement d’électrocoagulation. Le nombre d’échantillons ainsi que les temps entre prélèvements sont similaires à ceux réalisés pour l’électrocoagulation.
Le coagulant minéral choisi est le chlorure ferrique hexahydraté (FeCl3•6H2O) sous forme solide (fournisseur : Fisher Scientific Labosi) du fait que les électrodes utilisées en électrocoagulation sont en fer. La quantité de chlorure ferrique ajoutée à chaque étape de la cinétique est calculée sur la base des résultats des essais d’électrocoagulation. La même quantité de fer équivalente en chlorure ferrique obtenue après un temps d’électrocoagulation de 15 minutes est ajoutée toutes les 15 minutes pendant 120 minutes.
Les émulsions sont préparées à partir d’une huile de coupe algérienne (TASFALOUT 22/B) commercialisée par NAPHTAL. Elle est composée d’une huile minérale de base naphténique (80 %), d’émulgateurs anioniques, sulfonate de sodium (10 %), de cotensioactifs, alcool benzylique (5-6 %) et d’additifs divers (4 %).
La densité de l’huile de coupe est de 0,90, sa viscosité dynamique à la température de 50 °C est de 2,92 Pa.s et sa viscosité cinématique à 40 °C est de 28,8 mm2•s‑1 (cst).
Afin d’augmenter la conductivité électrique des émulsions, nous avons ajouté du chlorure de sodium (NaCl) à une concentration de 2,5 10‑2 mol•L‑1, soit 1,5 g•L‑1 (CHEN, 2004). Cela nous a permis d’obtenir des valeurs de conductivités plus élevées. Cet ajout est suffisant pour rendre le milieu conducteur mais insuffisant pour déstabiliser les émulsions traitées. Les caractéristiques des émulsions utilisées sont données par le tableau 1.
Tableau 1
Caractéristiques des émulsions utilisées.
Characteristics of the emulsions used.
Concentrations en huile % (p/p) |
1 |
2 |
4 |
|---|---|---|---|
Turbidité (NTU) |
170.102 |
210.102 |
610.102 |
pH |
9 |
9,09 |
9,28 |
Conductivité avant ajout de NaCl (ms•cm‑1) |
0,16 |
0,27 |
0,57 |
Conductivité après ajout de NaCl (ms•cm‑1) |
3,02 |
3,10 |
3,21 |
Les analyses ont été effectuées par la mesure de la turbidité à l’aide d’un turbidimètre de type HACH (Model 2100A); la mesure de la conductivité à l’aide d’un conductimètre TACUSSEL (type CDRV62); le spectre granulométrique des émulsions à l’aide d’un granulomètre laser MASTERSIZER 2000 (MALVERN, instruments) et la mesure du pH à l’aide d’un pHmètre type HI 9023 microcomputer. La pesée des électrodes avant et après chaque essai d’électrocoagulation est effectuée au moyen d’une balance de type SARTORIUS. Les électrodes sont conditionnées avant chaque manipulation afin de les décaper superficiellement (dégraissage par la soude puis décapage à l’acide sulfurique). Tous les essais d’électrocoagulation et de coagulation-floculation ont été réalisés deux fois afin de vérifier la reproductibilité des déstabilisations obtenues.
Le rendement de chaque procédé est évalué par la mesure de la turbidité liée à la concentration des microgouttelettes d’huile de coupe dans le mélange huile/eau (BENSADOK et al., 2008; CHEN-LU YANG, 2007; PINOTTI et al., 1999; RAJINDER et al., 1994; RIOS et al., 1998; ZOUBOULIS et al., 2000).
Le taux de réduction en turbidité de l’eau huileuse est exprimé par l’expression :
où T0 représente la turbidité initiale de l’émulsion et T la turbidité finale de l’émulsion.
Quant à la concentration en fer dissous en fonction du temps sous l’action de l’électrolyse, elle peut être calculée par la loi de Faraday. Cette loi permet d’accéder à la quantité théorique de fer dissous à l’anode connaissant la quantité d’électricité utilisée dans le réacteur. La quantité de fer dissous (FEUILLADE et al., 2001) est calculée par l’expression :
où m représente la masse de fer dissous, I l’intensité de courant, M la masse molaire du fer, F la constante de Faraday et Ne le nombre d’électrons mis en jeu dans la réaction.
Par contre, la quantité réelle de fer consommée a été mesurée expérimentalement par la pesée de l’anode avant et après l’essai d’électrocoagulation à l’aide d’une balance de type Sartorius et donnée par la relation suivante :
où m représente la quantité de fer consommée, m1 la masse de l’anode de fer avant l’essai d’électrocoagulation et m2 la masse de l’anode de fer après l’essai d’électrocoagulation.
Avant chaque essai les électrodes sont nettoyées (dégraissage à la soude puis décapage à l’acide sulfurique).
L’efficacité de courant (current efficiency (CE)), ou le rendement faradique pour la dissolution du métal (fer dans notre cas) est égal au rapport entre les quantités de fer dissous réellement et celles prévues par la loi de Faraday. Cette efficacité de courant (CE) est le rapport de la masse expérimentale de l’électrode consommée (Feexp) et la masse théorique (Fethé), donnée par la loi de Faraday, elle est définie par la relation suivante (XEMIMG CHEN et al., 2000) :
3. Résultats et discussion
3.1 Essais d’électrocoagulation
3.1.1 Influence de la densité de courant
Les essais d’électrocoagulation sur des échantillons d’huile de coupe Tasfalout 22/B ont été réalisés dans les conditions suivantes :
densités de courant (A•m‑2) : 50, 80, 100, 150, 200, 250, 300 et 350.
concentrations de l’émulsion : 1 % (p/p), 2 %(p/p) et 4 %(p/p)
temps d’électrolyse constant : 15 min.
ajout de NaCl telle que la concentration de la solution, soit de 1,5 g•L‑1.
Les essais d’électrocoagulation sur les émulsions d’huile de coupe sont réalisés sans correction du pH.
L’évolution de l’efficacité du procédé d’électrocoagulation en fonction de la densité de courant pour les différentes concentrations (1 % (p/p); 2 % (p/p) et 4 % (p/p)) est représentée sur la figure 1. Celle-ci montre, quelle que soit la concentration de l’émulsion, qu’une augmentation de la densité de courant entraîne une augmentation de l’efficacité du procédé. Cette croissance du rendement d’élimination est influencée par la densité de courant, qui ne détermine pas seulement la quantité de coagulant généré in situ, mais aussi la quantité de bulles de gaz produites (HOLT et al., 2005). Ceci peut aussi s’expliquer par le fait que la quantité des ions Fe2+ générée par la dissolution de l’anode augmente avec la densité de courant (loi de Faraday (équation 16). Il a été établi expérimentalement que, pour un temps donné, l’efficacité d’élimination augmente avec l’augmentation de la densité de courant. La quantité d’ions Fe2+ et Fe3+ est élevée, ce qui entraîne une quantité élevée de précipités d’hydroxydes, qui adsorberont les microgouttelettes d’huile, ce qui favorisera la déstabilisation de l’émulsion (ADHOUM et MONSEL, 2004; KHEMIS et al., 2006; KOBYA et al., 2003).
Figure 1
Efficacité de l’EC en fonction des densités de courant à différentes concentrations d’huile (te = 15 min).
Efficiency of electrocoagulation (EC) as a function of current densities at different oil concentrations. (t = 15min).
Par ailleurs, il a été montré que la densité des bulles de gaz augmente avec l’augmentation de la densité de courant et leur taille diminue (KETBAR et al., 1988; KETBAR et al., 1991; KHOSLA et al., 1991; SHEN et al., 2003); ceci entraîne un effet de flottation des flocs huileux et la formation d’une espèce de mousse à la surface libre du bécher d’essai.
Les études récentes (SAUR et al., 1996; HOSNY et al., 1996) montrent que la présence de NaCl diminue la taille des bulles de gaz, spécialement l’hydrogène. En effet, le chlorure de sodium augmente la tension superficielle, ce qui rigidifie l’interface gaz liquide et, par conséquent, limite la coalescence des bulles de gaz (KOIDE et al., 1968; MARRUCCI et NICODEMO, 1967; OLIVEIRA et al., 1999; STRICKLAND, 1980). La vitesse ascensionnelle des petites bulles est plus faible que celle des bulles plus larges (BRANDON et al., 1985).
La vitesse ascensionnelle d’une bulle de gaz (Vb) dans l’eau en régime laminaire est proportionnelle au carré du diamètre de la bulle de gaz, et elle est donnée par la loi de Stockes :
où db représente le diamètre de la bulle de gaz, ρg la masse volumique du gaz, ρl la masse volumique du liquide, η la viscosité dynamique et g l’accélération due à la pesanteur.
La vitesse ascensionnelle de la bulle de gaz est donc d’autant plus faible que le diamètre des bulles de gaz diminue. De ce fait, elles s’élèvent lentement vers la surface, ce qui augmente leur probabilité de collision avec les gouttelettes d’huile, ce qui conduit à une amélioration du procédé d’élimination des huiles. Ces auteurs indiquent que les microbulles d’hydrogène sont chargées positivement et elles peuvent neutraliser les polluants, dans notre cas les microgouttelettes chargées négativement par les tensioactifs anioniques. Par contre, l’ajout de NaCl n’influence pas la taille des gouttelettes (Figure 2) : distribution de la taille des gouttelettes pour (2 % (p/p)) et (2 % (p/p)) + NaCl à 1,5 g•L‑1). Cette stabilité de la taille des gouttelettes est due à la faible concentration en NaCl (1,5 g•L‑1), en effet, il faut atteindre des concentrations en NaCl de l’ordre de 20 g•L‑1 pour provoquer la déstabilisation de ces émulsions (SHUCAI, 1990).
Figure 2
Distribution de la taille des gouttelettes pour 2 % (p/p) et (2 % (p/p) + NaCl à 1,5 g•L‑1).
Drops size distribution for 2% (w/w) and 2% (w/w) + NaCl at 1.5 g•L‑1 emulsions.
3.1.2 Effet du pH et de la conductivité
La figure 3 représente l’évolution du pHfinal en fonction de la densité de courant pour les différentes concentrations.
Figure 3
Variation du pHfinal en fonction des densités de courant à différentes concentrations d’huile (te = 15 min).
Final pH variation in relation to current densities at different oil concentrations (t = 15 min).
Nous remarquons que le pH augmente régulièrement au cours du processus d’électrocoagulation jusqu’à un pH très basique. Cette augmentation du pH est due à la formation à la cathode d’ions hydroxydes provenant de la réaction de réduction des molécules (équation 7).
Nous constatons que l’emploi d’électrodes de fer conduit à la formation de flocs de couleur verte au niveau de l’anode à un pH basique, signe de la formation d’hydroxydes ferreux (équation 6).
Par contre, en phase aqueuse, les ions Fe2+ sont oxydés en ions Fe3+ par l’oxygène dissous et on constate la formation d’hydroxyde ferrique Fe (OH)3 de couleur rouille, selon la réaction :
Des chercheurs ont montré que durant le processus d’électrocoagulation, le pH de l’eau augmente approximativement d’une unité (ABUZAID et al., 2002; RUBACH et SAUR, 1997). De même l’augmentation du pH est due au dégagement de l’hydrogène à la cathode (VIK et al., 1984).
L’augmentation de la densité de courant est accompagnée par une augmentation de la conductivité électrique finale de la solution qui serait due aux ions hydroxydes (OH-) libérés pendant le processus d’électrocoagulation.
3.1.3 Effet du temps d’électrocoagulation
Nous avons suivi la cinétique de dissolution de l’électrode en fer pour une période de 120 min avec une densité de courant de 50, 100 et 150 A•m‑2 pour les différentes concentrations d’huile de coupe (1 % (p/p), 2 % (p/p) et 4 % (p/p)).
L’effet du temps sur la turbidité de l’émulsion à 2 % (p/p) est résumé sur la figure 4. Nous constatons que le temps d’électrolyse joue un rôle prépondérant et a un effet remarquable sur l’efficacité du traitement. Le taux d’élimination en turbidité augmente en fonction du temps d’électrolyse. Cette augmentation d’efficacité s’explique par une élimination de l’huile adsorbée dans les flocs, dont la quantité augmente, qui vont être entraînés vers la surface par les microbulles de gaz produites au cours de l’opération.
Figure 4
Effet du temps sur l’efficacité de l’EC à différentes densités de courant pour 2 % (p/p).
Effect of time on EC efficiency at different current densities for the 2% (w/w) emulsion.
L’électrocoagulation d’une eau usée huileuse, avec une anode sacrifiée en fer a été étudiée (IBANEZ et al., 1995). Cette anode est oxydée en Fe2+ qui est ensuite oxydée en Fe3+, selon les étapes suivantes :
L’émulsion d’huile de coupe est stabilisée par la présence d’agents émulsifiants, en général des tensioactifs anioniques. Ces tensioactifs sont localisés au niveau de l’interface huile/eau des microgouttelettes. La partie non polaire (queue du tensioactif) est dissoute dans l’huile et l’autre partie qui est la partie polaire (tête du tensioactif) est dissoute dans la phase aqueuse. Les ions ferreux et ferriques avec une charge positive élevée neutralisent la charge de surface négative des ions tensioactifs anioniques. Simultanément, l’hydrogène est dégagé à la cathode (équation 7).
Selon les deux réactions ci-dessus (équations 7 et 21) l’émulsion est déstabilisée et les microgouttelettes commencent à coalescer sous l’effet de leur mouvement brownien (coagulation péricinétique).
À la fin, les gouttelettes d’huiles déstabilisées s’adsorbent sur le floc d’hydroxyde formé par la réaction entre le Fe3+ et OH-, soit :
Lors de l’électrocoagulation il y a formation de flocs de type mousse du fait qu’il y a interaction entre un floc d’hydroxyde ferrique Fe (OH)3 , les micro-gouttelettes d’huile déstabilisées et les microbulles de gaz (oxygène et hydrogène) formées au niveau des électrodes. Les microbulles de gaz se trouvent ainsi piégées au sein d’un floc huileux d’hydroxyde ferrique, constituant ainsi une mousse en surface du bécher. Cette mousse sera facilement éliminée par écumage.
Nous remarquons que la même efficacité du procédé peut être obtenue par diminution du temps d’électrolyse et une augmentation de la densité de courant (Figure 4). À titre d’exemple, un rendement de 79 % est obtenu avec un temps d’électrolyse de 90 min, et une densité de courant de 50 A•m‑2; ce même rendement est aussi obtenu pour un temps d’électrolyse de 60 min et une densité de courant de 150 A•m‑2. Ces résultats sont en accord avec ceux trouvés (XUEMING CHEN et al., 2000; ADHOUM et MONSEL, 2004) qui ont montré que si la densité de courant diminue, le temps nécessaire pour obtenir la même efficacité augmente. Ce résultat expérimental est aussi expliqué par le fait que l’efficacité de traitement est principalement affectée par la quantité d’électricité mise en oeuvre (q = It) (XUEMING CHEN et al., 2000). De même, pour un temps d’électrolyse donné, l’efficacité d’élimination augmente significativement avec l’augmentation de la densité de courant. Ainsi, pour un temps d’électrolyse de 60 min et une densité de courant de 50 A•m‑2, nous avons un rendement de 50 %. Par contre, pour une densité de courant trois fois plus élevée que la précédente (150 A•m‑2) et un temps d’électrolyse de 60 min; nous avons un rendement de 79 % (Figure 4).
La figure 5 représente l’évolution du pHfinal en fonction du temps pour la concentration en huile à 2 % (p/p) et les densités de courant de 50 A•m‑2 et 100 A•m‑2.
Figure 5
Variation du pHfinal en fonction du temps pour (2 % (p/p); i = 50 A•m‑2 et i = 100 A•m‑2).
Final pH variation in relation to time for the 2% (w/w) emulsion; i = 50 A•m‑2 and i = 100 A•m‑2.
Nous constatons que le pH augmente régulièrement au cours du processus d’électrocoagulation jusqu’à un pH basique. Cette augmentation du pH est due à la formation à la cathode d’ions hydroxydes provenant de la réaction de réduction des molécules d’eau (Équation 7).
3.1.4 Effet de la masse du coagulant (Fe2+)
La masse en coagulant mis en solution est liée au temps d’application du champ électrique, calculée à partir de la loi de Faraday. L’efficacité de courant (CE) ou le rendement Faradique est le rapport entre la masse expérimentale de l’électrode consommée (Feexp) et la masse théorique (Fethe). La pesée de l’anode avant et après l’essai d’électrocoagulation et l’application de la loi de Faraday sur l’émulsion d’huile de coupe, a donné des valeurs de CE comprises entre 70 % et 112 % pour les différentes concentrations à différentes densités de courant. Nous constatons, suivant l’efficacité de courant, que la loi de Faraday est applicable. L’écart existant entre les valeurs de la masse prévue et celle de la masse expérimentale dans certains cas est dû à la perturbation du processus causée par la variation de l’intensité du courant lors de l’expérimentation.
La quantité de fer générée durant l’électrolyse excède, dans certains cas, la valeur théorique calculée à partir de la loi de Faraday. Les valeurs de l’efficacité de courant qui ont été rapportées par la littérature pour des électrodes en aluminium sont comprises entre 109 et 215 % (CHEN et al., 2002; SHEN et al., 2003).
Des recherches ont montré que la masse du métal anodique dissous dans la solution peut augmenter ou diminuer par rapport à la valeur théorique, et ce, à cause des caractéristiques de l’eau brute et des conditions opératoires (pH de l’électrolyse, intensité de courant, durée de l’électrolyse, etc.). Selon les résultats expérimentaux (XUEMING et al., 2000) une perte de masse de 16,52 g a été trouvée pour une valeur théorique de 13,91 g, soit une efficacité de courant de 118,8 %.
Cet écart est aussi dû à la réduction et à l’oxydation électrochimique (équations 7 et 10), qui entraîne la dissolution chimique des électrodes de fer respectivement près de la cathode et de l’anode (causée par la vitesse de dissolution chimique élevée, qui se produit pour des pH alcalins et acides) (JIANG et al., 2002; PICARD et al., 2000; SZPYRKOWICZ, 2005).
Ce point de vue n’est pas partagé par d’autres auteurs qui suggèrent que l’excès en efficacité de courant (> 100 %) est expliqué par la corrosion par piquage (pitting corrosion) de l’anode en aluminium, causée par la présence d’ions chlorure dans le milieu (KHEMIS et al., 2006; MAMERI et al., 1998; SHEN et al., 2003).
La loi de Faraday joue un rôle important dans le processus d’électrocoagulation, surtout en ce qui concerne la détermination de la masse du métal anodique dissous dans la solution, ce qui permet de connaître la durée de vie des électrodes.
3.1.5 Description visuelle du procédé
Pendant le processus d’électrocoagulation on observe les phénomènes suivants :
Une agitation de l’émulsion due à l’attraction des microgouttelettes vers l’anode;
Un dégagement gazeux au voisinage des deux électrodes, l’hydrogène (H2) à la cathode et l’oxygène (O2) à l’anode, ces microbulles de gaz participent à l’agitation et l’hydrogène évite la formation de dépôt sur la cathode;
Une formation lente des flocs;
L’apparition de mousse à la surface de la solution à traiter, le dégagement d’oxygène d’hydrogène forme ces mousses abondantes, qui entraînent les flocs huileux vers la surface et favorisent la récupération des boues par flottation;
Une flottation des flocs formés de plus en plus marqués en fonction du temps, de couleur verdâtre (présence de Fe(OH)2( s)) et de couleur rouille (présence de Fe(OH)3(s)) à pH basique (LARUE et al., 2003);
Une certaine quantité de boue décante à la fin de l’essai.
En fin d’opération, on observe un dépôt de flocs sur l’anode. Ces flocs sont de couleur verte (présence de Fe (OH)2(s), pH basique).
3.2 Comparaison entre la coagulation floculation et l’électrocoagulation.
La masse (m1) en chlorure ferrique hydratée équivalente à la masse (m) de fer dissous est donnée par la relation suivante :
où MFeCl3•6H2O représente la masse molaire du chlorure ferrique, MFe la masse de l’ion fer et m la masse de fer dissous.
La masse en fer (m) et la masse équivalente en (FeCl3•6H2O) (m1) pour un temps de traitement de 15 min sont données par le tableau 2. Les valeurs de (m) du tableau 2a sont les résultats des expériences d’électrocoagulation réalisées. Ces valeurs permettent d’obtenir les masses équivalentes en chlorure ferrique (m1). Le tableau 2b, par contre, donne les valeurs des masses en fer données à partir de la loi de Faraday.
Tableau 2
Masses en fer (m) et masses équivalentes en (FeCl3, 6 H2O) (m1) (i = 50; 100 et 150 A•m‑2; te = 15 min). (a) : masses expérimentales en fer données par la pesée (m) et masses équivalentes en (FeCl3•6 H2O) (m1). (b) : masses théoriques en fer données par la loi de Faraday (m) et masses équivalentes en (FeCl3•6 H2O) (m1).
Masses of iron (m) and equivalent masses of (FeCl3•6H2O) (m1) (i = 50, 100 et 150 A•m‑2; t = 15 min). (a): experimental masses of iron given by the weight (m) and equivalent masses of (FeCl3•6H2O) (m1). (b): theoretical masses of iron given by Faraday’s law (m) and equivalent masses of (FeCl3•6H2O) (m1).
(a)
i (A•m‑2) |
50 |
100 |
150 |
|---|---|---|---|
m (g) |
0,1 |
0,2 |
0,3 |
m1 (g) |
0,48 |
0,97 |
1,45 |
(b)
i (A•m‑2) |
50 |
100 |
150 |
|---|---|---|---|
m (g) |
0,091 |
0,182 |
0,271 |
m1 (g) |
0,44 |
0,88 |
1,31 |
Les masses équivalentes en chlorure ferrique qui sont utilisées en coagulation-floculation sont celles du tableau 2a.
La coagulation-floculation a été suivie pendant une durée de 120 minutes. Les résultats expérimentaux obtenus par le procédé de coagulation-floculation et d’électrocoagulation pour l’émulsion à 1 % (p/p) pour les différentes densités de courant (50 A•m‑2; 100 A•m‑2 et 150 A•m‑2) montrent l’effet marqué de la quantité de chlorure ferrique introduite ou formée in situ pour chacun des deux procédés. Plus la concentration en fer est élevée, plus le rendement d’élimination de l’huile est élevé. Ces résultats ont pu être vérifiés par des travaux dans le cas de la coagulation floculation montrant que la turbidité finale diminue en fonction du temps pour une huile de coupe, en utilisant comme coagulant minéral du CaCl2 et du AlCl3. Selon ces auteurs, la diminution de la turbidité finale est due à la collision des gouttelettes d’huile suivie de leur coalescence qui entraîneraient une diminution du nombre des gouttelettes. Le processus est principalement contrôlé par le nombre de collisions gouttelettes-gouttelettes (RIOS et al., 1998).
Nous constatons que dans le cas de l’émulsion à 1 % (p/p) la moins concentrée, l’efficacité de déstabilisation est plus importante pour la coagulation-floculation par rapport à l’électrocoagulation, pour les différentes densités de courant.
Les figures 6 et 7 montrent les résultats obtenus par le procédé d’électrocoagulation et de coagulation-floculation pour l’émulsion à 2 % (p/p), respectivement pour les densités de courant de 100 et 150 A•m‑2.
Figure 6
Comparaison entre les deux procédés pour (2 % (p/p); i = 100 A•m‑2; m1* = 0,97 g).
Comparison between the two processes for the 2% (w/w) emulsion; i = 100 Am‑2; m*1 = 0.97 g.
Figure 7
Comparaison entre les deux procédés pour (2 % (p/p); i = 150 A•m‑2; m1** = 1,45g).
Comparison between the two processes for the 2% (w/w) emulsion; i = 150 A•m‑2; m1** = 1.45 g.
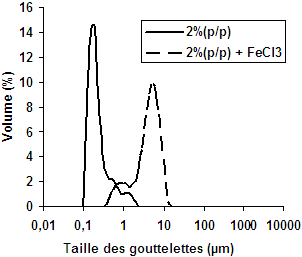
L’effet de la quantité de fer sur les deux procédés est très visible. L’ajout de FeCl3•6H2O influence la taille des gouttelettes d’huile. La figure 8 représente la distribution de la taille des gouttelettes après addition de (FeCl3•6H2O) à l’émulsion à 2 % (p/p); nous observons une augmentation de la taille des gouttelettes, ceci étant dû à une coalescence gouttelettes- gouttelettes.
Figure 8
Distribution de la taille des gouttelettes pour 2 % (p/p) et (2 % (p/p) + FeCl3•6H2O).
Drop size distribution for the 2% (w/w) and 2% (w/w) + FeCl3•6H2O emulsions.
L’efficacité de déstabilisation de l’émulsion est plus importante pour le procédé de coagulation-floculation que pour l’électrocoagulation pour la densité de courant de 100 A•m‑2 (Figure 6). Par contre, pour la densité de courant de 150 A•m‑2, les rendements de l’électrocoagulation sont sensiblement similaires à ceux de la coagulation-floculation (Figure 7). Cette différence peut-être attribuée a la production de microbulles de gaz. La densité de courant influence l’effet d’électrolyse et, de ce fait, l’effet de flottation dû aux microbulles de gaz (KETBAR et al., 1988; KETBAR et al., 1991). De même une augmentation dans l’intensité de courant entraîne une diminution de la taille des bulles de gaz (CHEN et al., 2002; SHEN et al., 2003). La vitesse ascensionnelle des petites bulles est plus faible que des bulles plus grosses (BRANDON et al., 1985). Elles s’élèvent lentement vers la surface, ce qui augmente leur probabilité de collision avec les gouttelettes d’huile. De plus, la quantité de fer libéré est plus élevée pour une densité de courant de 150 A•m‑2 entraînant une amélioration du procédé d’élimination des huiles par électrocoagulation.
Les résultats obtenus par le procédé d’électrocoagulation et de coagulation-floculation pour l’émulsion à 4 % (p/p), pour les densités de courant de 100 et 150 A•m‑2, montrent aussi l’influence de la quantité de fer introduite ou générée respectivement pour les deux procédés.
Pour la densité de courant de 100 A•m‑2, l’efficacité de déstabilisation de l’émulsion est importante pour le procédé de coagulation-floculation; par contre, pour la densité de courant de 150 A•m‑2, les rendements d’élimination des deux procédés sont aussi sensiblement similaires comme dans le cas de l’émulsion à 2 % (p/p). Ces résultats sont en accord avec ceux trouvés (CANIZARES et al., 2008) montrant que les efficacités en électrocoagulation et en coagulation-floculation sont sensiblement similaires pour des concentrations élevées en aluminium.
La figure 9 représente le pHfinal en fonction du temps, pour l’émulsion à 1 % (p/p) dans le cas de la coagulation-floculation, pour les différentes masses. Nous constatons que le pH diminue rapidement; il passe de 9,08 à 3,32 après 15 minutes de coagulation-floculation. Il a été montré que les flocs générés par (FeCl3 6H2O) commencent à précipiter autour d’un pH de 3 (LARUE et al., 2003).
Figure 9
pHfinal en fonction du temps en coagulation- floculation pour 1 % (p/p).
Final pH in as a function of time for the coagulation flocculation of the 1% (w/w) emulsion.
De même, nous pouvons affirmer que le pH diminue dès l’introduction du coagulant minéral, par suite de l’hydrolyse du chlorure ferrique (sel faible). L’introduction de (FeCl3, 6 H2O) entraîne une acidification du milieu selon la réaction d’hydrolyse suivante :
Le milieu devient acide dans le cas de la coagulation floculation et il reste basique dans le cas de l’électrocoagulation.
La comparaison directe entre l’électrocoagulation et la coagulation chimique n’est pas simple à réaliser car les deux procédés opèrent différemment. La quantité de fer est introduite ou générée in situ par oxydation électrolytique de l’anode respectivement pour les deux procédés. Le pH des émulsions obtenu après le traitement pour les deux procédés est différent, celui-ci peut influencer le mode opératoire (CANIZARES et al., 2008; FEUILLADE et al., 2001).
La procédure d’élimination de la pollution est également différente, alors que la coagulation-floculation conduit généralement à la décantation de la pollution, l’électrocoagulation entraîne une décantation et également une flottation de la pollution par les microbulles de gaz produites à la cathode et à l’anode.
4. Conclusion
Le premier objectif de ce travail est de montrer l’intérêt du procédé d’électrocoagulation pour le traitement d’une émulsion d’huile de coupe algérienne (Tasfalout 22/B), très stable et caractérisée par une turbidité élevée.
Des essais d’électrocoagulation ont été réalisés en batch, en utilisant des électrodes de fer. Ces essais ont permis de montrer l’influence de la densité de courant dans le processus d’électrocoagulation. Une meilleure efficacité du procédé est observée, pour les trois concentrations en huile, si l’on augmente la densité de courant.
De même, le suivi de la cinétique de dissolution de l’électrode de fer sur une période de 120 min a montré que, pour la même efficacité d’électrocoagulation, une densité de courant plus élevée entraîne une diminution du temps d’électrolyse. Nous constatons aussi que, pour un temps d’électrolyse donné, l’efficacité d’élimination augmente significativement avec l’augmentation de la densité de courant. Ces deux constatations montrent clairement que le paramètre clé qui conditionne l’électrocoagulation est la quantité d’électricité q = it.
L’efficacité d’élimination en turbidité est importante (99 %), pour une émulsion à 4 % (p/p), une densité de courant de 150 A•m‑2 et un temps d’électrolyse de 120 min; mais la turbidité finale reste supérieure aux normes de rejet. De ce fait, le procédé d’électrocoagulation pourrait être un procédé de prétraitement avant un procédé membranaire.
Une étude comparative entre le procédé de coagulation-floculation et d’électrocoagulation pour différentes densités de courant a permis de montrer l’avantage du procédé de coagulation-floculation pour l’émulsion à 1 % (p/p). Des rendements d’élimination de l’huile sensiblement similaires ont été trouvés pour les deux procédés, pour les concentrations en huile de coupes élevées, pour une densité de courant de 150 A•m‑2.
Parties annexes
Références bibliographiques
- ABUZAID J.S., A.A. BUKHARI et Z.M. AL-HAMOUZ (2000). Ground water coagulation using soluble stainless steel electrodes. Adv. Environ. Res., 6, 325-333.
- ADHOUM N. et L. MONSER (2004). Decolourization and removal of phenolic compound from olive mill wastewaters by electrocoagulation. Chem. Eng. Process., 43, 1281-1287.
- AMOSOV V.V., A.G. ZIL’BRTMAN et al. (1976). Experience in local treatment of wastewaters from petrochemical production. Chem. Technol. Fuel Oils, 12, 11-12, 850-852.
- BAKLAN V.Y et I.P. KOLESNIKOVA (1996). Influence of electrode material on the electrocoagulation. J. Aerosol Sci., 27, supplement 1: S209-S210.
- BENSADOK K., S. BENAMAR, F. LAPICQUE et G. NEZZAL (2008). Electrocoagulation of cutting oil emulsions using aluminium plate electrodes. J. Hazard. Mater., 152, 423-430.
- BRANDON N.P., G.H. KELSALL, S. LEVINE et A.L. SMITH (1985). Interfacial electrical properties of electrogenerated bubbles. J. Appl. Electrochem., 15, 485-493.
- Cañizares P. F. Martínez, C. Jiménez, C. Sáez et M.A. Rodrigo (2008). Coagulation and electrocoagulation of oil in water emulsion. J. Hazard. Mater., 151, 44-51.
- CHEN G. (2004). Electrocoagulation technologies in wastewater treatment. Sep. Purif. Technol., 38, 11-41.
- CHEN-LU YANG (2007). Electrochemical coagulation for oily water demulsification. Sep. Purif. Technol., 54, 388‑395.
- CHEN X., G. CHEN et P.L. YUE (2002). Novel electrode system for electroflotation wastewater. Environ.Sci.Technol. 36, 778-783.
- DANESHVAR N., H. ASHASSI-SOKHABI et A. TIZPAR (2003). Decolorization of orange by electrocoagulation method. Sep. Purif. Technol., 31, 153-162.
- DO J.S. et M.L. CHEN (1994). Decolourization of dye-containing solutions by electrocoagulation. J. Appl. Electrochem., 24, 785-790.
- FEUILLADE G., S. GUERAUDE, Y. BRIZARD et C. LAHITTE (2001). L’électrocoagulation et la production d’eau potable; faisabilité, intérêt et performance. Dans : 4e Congrès International Gruttee. 22-23 novembre 2001. Limoges.
- HOLT P.K., G.W. BARTON et C.A. MITCHELL (2005). The future for electrocoagulation as a localized water treatment technology. Chemosphere, 59, 355-367.
- HOSNY A.Y. (1996). Separation oil from oil-water emulsion by electroflotation. Sep. Technol., 6, 9-17.
- HULSER P., U.A. KRUGER et F. BECK (1996). The cathodic corrosive of aluminum during the electrodeposition of paint: electrochemical measurements. Corrosion. Sci., 38, 47-57.
- IBANEZ J.G, M.M. TAKIMOTO et R.C. VASQUEZ (1995). Laboratory experiment on electrochemical remediation of the environment: electrocoagulation of oily wastewater. J. Chem. Educ., 72, 1050-1052.
- IBANEZ J.G., M.H. SINGH et Z. SZAFRA (1998). Laboratory experiments on electrochemical remediation of the environment. Part 4: color removal of simulated wastewater by electrocoagulation- electroflotation. J. Chem. Educ., 75, 1040-1041.
- JIANG J.Q., N. GRAHAM, C.A. ANDRE, G.H. KELSALL et N. BRANDON. Laboratory study of electro-coagulation-flotation for water treatment. Water Res., 36, 4064-4078.
- KETBAR D.R., R. MALLIKARJUNAN et S. VENKATACHALAM (1988). Size determination of electro generated gas bubbles. J. Electrochem. Soc. India, 37, 313.
- KETBAR D.R., R. MALLIKARJUNAN et S.VENKATACHALAM (1991). Electroflotation quartz fines. Intern. J. Min. Process., 31, 127-138.
- KHEMIS M., J.P. LECLERC, G. TANGUY, G. VALENTIN et F. LAPICQUE (2006). Treatment of industrial liquid wastes by electrocoagulation. Experimental investigations and an interpretation model. Chem. Eng. Sci., 61, 3602‑3609.
- KHOSLA N.K., S. VENKACHALAM et P. SONRASUNDARAM. Pulsed electrogeneration of bubbles for electroflotation. J. Appl. Electrochem., 21, 986‑990.
- KOBYA M., O.T. CAN et M. BAYRAMOGLU (2003). Treatment of textile wastewaters by electrocoagulation using iron and aluminium electrodes. J. Hazard. Mater., B100, 163-178.
- KOIDE K., S. KATOS, Y. TANAKA et H. KUBOTA (1968). Bubble generated from porous plate. Chem. Eng. Sci., 1, 51-56.
- LABANOWSKI J. et G. FEUILLADE (2006). Étude de la matière organique réfractaire à la coagulation floculation et à son procédé alternatif, l’électrocoagulation, lors du traitement d’un lixiviat stabilisé. Déchets Sci. Tech., 41, 10‑14.
- LARUE O., E. VOROBIEV, C. VU et B. DURAND (2003). Electrocoagulation and coagulation by iron of latex particles in aqueous suspensions. Sep. Purif. Technol., 31, 177-192.
- MAMERI N., A.R. YEDDOU, H. LOUNICI, D. BELHOUCINE, H. GRIB et B. BARIOU (1998). Defluoridation of septentrional Sahara water of North Africa by electrocoagulation process using bipolar aluminum electrodes. Water Res., 32, 1604‑1612.
- MARRUCCI G. et L. NICODEMO (1967). Coalescence of gaz bubbles in aqueous solutions of inorganics electrolytes. Chem. Eng.Sci., 22, 1257-1265.
- MATTESON M.J., R.L. DOBSON, R.W. GLENN, N.S. KUKUNOOR, W.H. WAITS et E.J. CLAYFIELD (1995). Electrocoagulation and separation of aqueous suspensions of ultrafine particles. Colloid. Surf. A: Physicochem. Eng. Aspects, 104, 101-109.
- MOLLAH M.A., R. SCHENNAC, J.R. PARGA et D.L. COCKE (2001). Electrocoagulation (EC). Science and application . J. Hazard. Mater., B.84, 29-41.
- NIKOLAEV N.V., A.S. KOZLOVSKI et I.I. UTKIN (1982). Treating natural waters in small water systems by filtration with electrocoagulation. Soviet J. Water Chem. Technol., 4, 244-247.
- NOVIKOVA S.P., T.L. SHKORBATOVA et E.Y. SOKOL (1982). Purification of effluents from the production of synthetic detergents by electrocoagulation. Soviet J. Water Chem. Technol., 4, 353-357.
- OLIVEIRA R.C.G., G.GONZALEZ et J.F. OLIVEIRA (1999). Interfacial studies on dissolved gas flotation of oil droplets for water purification. Colloids. Surf. A: Physicochem. Eng. Aspects, 154, 127-135.
- OSIPENKO V.D et P.I. POGORELYI (1977). Electrocoagulation neutralization of chromium containing effluent. Metallurgist, 21, 44-45.
- PICARD T., G. CATHALIFAUD-FEUILLADE, M. MAZET et C. VANDENSTEEDAM (2000). Cathodic dissolution in the electrocoagulation process using aluminium electrode. J. Environ. Monit., 2, 77-80.
- PINOTTI A. et N. ZARITZKY (2001). Effect of aluminium sulfate and cationic polyelectrolytes on the destabilization of emulsified wastes. Waste Manag., 21, 535-542.
- POURBAIX M. (1974). Atlas of electrochemical equilibria in aqueous solutions. 2e édition, Pergamon Press, Houston, 1974.
- RAJINDER P. (1994). Techniques for measuring the composition (oil and water content) – a state of the art review. Colloids Surf. A, 84, 141-193.
- RIOS G., C. PAZO et J. COCA (1998). Destabilisation of cutting oil emulsion using inorganic salts as coagulants. J.Colloids Surf., 138, 383-389.
- RUBACH S. et I.F. SAUR (1997). Onshore testing of produced waster by electrocoagulation. Filt. Sep., Octobre, 877-882.
- SAUR I.F., S. RUBACH, J.S. FORDE, G. KJAERHEIM et U. SYVERSEN (1996). Electroflocculation: removal of oil, heavy metal and organic compounds from oil-in-water emulsion. Filt. Sep., 33, 295-303.
- SHEN F., X. CHEN, P. GAO et G.CHEN (2003). Electrochemical removal of fluoride ions from industrial wastewater. Chem. Eng. Sci., 58, 987-993.
- SHUCAI Z. (1990). Étude des traitements physico-chimiques d’épuration des émulsions d’huile de coupe. Influence de leur formulation. Thèse de Doctorat, Institut National Des Sciences Appliquées de Toulouse, France, 195 p.
- STRICKLAND J.R. (1980). Laboratory results of cleaning produced water by gaz flotation. Soc. Petrol. Eng. J., June 1980, 175‑190.
- SZPYRKOWICZ L. (2005). Hydrodynamic effects on the performance of electro-coagulation/electro-flotation for the removal of dyes from textile wastewater. Ind. Eng. Chem. Res., 44, 7844-7853.
- VIK E.A., D.A. CARLSON, A.S. EIKUM et E.T. GLESSING (1984). Electrocoagulation of potable water. Water Res.,18, 1355-1360.
- XINHUA X. et XIANGFENG Z. (2004). Treatment of refectory oily wastewater by electro-coagulation process. Chemosphere, 56, 889-894.
- XUEMING C., GUOHUA C. et P. LOCK YUE (2000). Separation of polluants from restaurant wastewater by electrocoagulation. Sep. Purif. Technol., 19, 65-76.
- ZOUBOULIS A.I. et A. AVRANAS (2000). Treatment of oil-in-water emulsion by coagulation and dissolved-air flotation. Colloids Surf. A: Physicochem. Eng. Aspects, 172, 153-161.
Liste des figures
Figure 1
Efficacité de l’EC en fonction des densités de courant à différentes concentrations d’huile (te = 15 min).
Efficiency of electrocoagulation (EC) as a function of current densities at different oil concentrations. (t = 15min).
Figure 2
Distribution de la taille des gouttelettes pour 2 % (p/p) et (2 % (p/p) + NaCl à 1,5 g•L‑1).
Drops size distribution for 2% (w/w) and 2% (w/w) + NaCl at 1.5 g•L‑1 emulsions.
Figure 3
Variation du pHfinal en fonction des densités de courant à différentes concentrations d’huile (te = 15 min).
Final pH variation in relation to current densities at different oil concentrations (t = 15 min).
Figure 4
Effet du temps sur l’efficacité de l’EC à différentes densités de courant pour 2 % (p/p).
Effect of time on EC efficiency at different current densities for the 2% (w/w) emulsion.
Figure 5
Variation du pHfinal en fonction du temps pour (2 % (p/p); i = 50 A•m‑2 et i = 100 A•m‑2).
Final pH variation in relation to time for the 2% (w/w) emulsion; i = 50 A•m‑2 and i = 100 A•m‑2.
Figure 6
Comparaison entre les deux procédés pour (2 % (p/p); i = 100 A•m‑2; m1* = 0,97 g).
Comparison between the two processes for the 2% (w/w) emulsion; i = 100 Am‑2; m*1 = 0.97 g.
Figure 7
Comparaison entre les deux procédés pour (2 % (p/p); i = 150 A•m‑2; m1** = 1,45g).
Comparison between the two processes for the 2% (w/w) emulsion; i = 150 A•m‑2; m1** = 1.45 g.
Figure 8
Distribution de la taille des gouttelettes pour 2 % (p/p) et (2 % (p/p) + FeCl3•6H2O).
Drop size distribution for the 2% (w/w) and 2% (w/w) + FeCl3•6H2O emulsions.
Figure 9
pHfinal en fonction du temps en coagulation- floculation pour 1 % (p/p).
Final pH in as a function of time for the coagulation flocculation of the 1% (w/w) emulsion.
Liste des tableaux
Tableau 1
Caractéristiques des émulsions utilisées.
Characteristics of the emulsions used.
Concentrations en huile % (p/p) |
1 |
2 |
4 |
|---|---|---|---|
Turbidité (NTU) |
170.102 |
210.102 |
610.102 |
pH |
9 |
9,09 |
9,28 |
Conductivité avant ajout de NaCl (ms•cm‑1) |
0,16 |
0,27 |
0,57 |
Conductivité après ajout de NaCl (ms•cm‑1) |
3,02 |
3,10 |
3,21 |
Tableau 2
Masses en fer (m) et masses équivalentes en (FeCl3, 6 H2O) (m1) (i = 50; 100 et 150 A•m‑2; te = 15 min). (a) : masses expérimentales en fer données par la pesée (m) et masses équivalentes en (FeCl3•6 H2O) (m1). (b) : masses théoriques en fer données par la loi de Faraday (m) et masses équivalentes en (FeCl3•6 H2O) (m1).
Masses of iron (m) and equivalent masses of (FeCl3•6H2O) (m1) (i = 50, 100 et 150 A•m‑2; t = 15 min). (a): experimental masses of iron given by the weight (m) and equivalent masses of (FeCl3•6H2O) (m1). (b): theoretical masses of iron given by Faraday’s law (m) and equivalent masses of (FeCl3•6H2O) (m1).
(a)
i (A•m‑2) |
50 |
100 |
150 |
|---|---|---|---|
m (g) |
0,1 |
0,2 |
0,3 |
m1 (g) |
0,48 |
0,97 |
1,45 |
(b)
i (A•m‑2) |
50 |
100 |
150 |
|---|---|---|---|
m (g) |
0,091 |
0,182 |
0,271 |
m1 (g) |
0,44 |
0,88 |
1,31 |