Résumés
Résumé
La transplantation hépatique permet de traiter les formes les plus graves de cirrhose, ainsi que certaines tumeurs malignes du foie (carcinomes hépatocellulaires de petite taille), avec une espérance de vie dépassant respectivement 70 % et 60 % à cinq ans. Les traitements immunosuppresseurs actuels permettent à la fois de prévenir le rejet chronique dans plus de 90 % des cas et d’assurer le plus souvent une excellente qualité de vie. Le facteur limitant principal est le manque de donneurs en état de mort cérébrale. En effet, malgré une sélection des candidats ayant les meilleures chances de succès, l’attente d’un greffon dure habituellement plusieurs mois et la mortalité en liste d’attente est de 10 % à 15 %. Le manque de donneurs a conduit à développer des alternatives à la transplantation conventionnelle, dont les principales sont les techniques du donneur vivant et du foie partagé. La transplantation par donneur vivant peut s’appliquer à environ 20 % à 30 % des candidats. Le greffon, bien qu’il soit initialement de petite taille, se régénère et retrouve une taille normale en quelques semaines. Les résultats en termes de survie sont équivalents à ceux de la transplantation par donneur cadavérique. Le risque pour le donneur doit être inférieur à 1 %, ce qui conduit à une sélection très attentive. Les donneurs ne peuvent être que des parents directs ou le conjoint. La technique du foie partagé repose sur le partage d’un greffon cadavérique en deux parties autonomes attribuées à deux receveurs. Bien qu’attractive, cette méthode ne peut être appliquée qu’à moins de 25 % des donneurs. L’incitation au don d’organes dans la population générale reste donc encore une priorité.
Summary
Liver transplantation allows to treat patients with end-stage cirrhosis as well as some liver malignancies (small size hepatocellular carcinoma) with a life expectancy exceeding 70 and 60 % at 5 years, respectively. Current immunosuppressive agents make it possible to prevent chronic rejection in more than 90 % of the patients and to preserve an excellent quality of life in most cases. The principal limiting factor for liver transplantation is represented by the scarcity of brain-dead donors. Indeed, despite the selection of those candidates who have the best chance of surviving after transplantation, several months are usually necessary for obtaining a graft and the mortality on the waiting list may reach 10 to 15 %. Organ shortage incited to develop alternatives to conventional transplantation, the most important of which are living donor transplantation and split liver transplantation. Living donor transplantation can be applied to about 20 to 30 % of candidates. Thought initially smaller, the partial graft regenerates and its volume is restored within a few weeks. The results of living donor transplantation in terms of survival are comparable to those of cadaveric transplantation. The risk for the donor has to be lower than 1 % which makes that selection must be especially cautious. Donors must be direct relatives or spouses. Split liver transplantation technique, based on the separation of a cadaveric graft into two functional parts transplanted in two distinct recipients, although attractive, is applicable to less than 25 % of the donors. Education for organ donation in the general population still remains a priority.
Corps de l’article
La transplantation hépatique reste l’unique moyen de pallier durablement les insuffisances hépatiques graves et leurs conséquences. En effet, il n’existe pas de technique de suppléance artificielle des fonctions hépatiques comparable à l’hémodialyse pour l’insuffisance rénale. Bien que la transplantation soit une intervention chirurgicale lourde, les progrès réalisés dans la sélection des candidats, les techniques chirurgicales et les traitements immuno- suppresseurs font que le taux de survie à un an excède en moyenne 80 %. Entre 700 et 800 transplantations hépatiques sont réalisées chaque année en France. Cependant, le manque de donneurs conduit au décès de 5 % à 15 % des candidats à la transplantation pendant la période d’attente.
Critères de sélection des receveurs
Le manque de donneurs conduit à sélectionner les candidats qui ont les meilleures chances de succès. La plupart des équipes écartent les candidats pour lesquels les chances de succès sont faibles (inférieures à 50 % à un an), considérant qu’il serait illogique d’attribuer un greffon à un malade ayant un pronostic réservé, alors que ce greffon aurait pu être attribué à un receveur ayant un meilleur pronostic.
Maladies chroniques non tumorales du foie
Les maladies parenchymateuses chroniques (cirrhoses) représentent les indications les plus fréquentes de la transplantation hépatique. Quelle que soit l’étiologie de la cirrhose, une transplantation est envisagée lorsqu’il existe à la fois une insuffisance hépatique sévère (taux de prothrombine inférieur à 50 %) non réversible et une ou plusieurs complications graves, telles qu’une ascite réfractaire, une infection du liquide d’ascite, une encéphalopathie chronique ou des hémorragies digestives récidivantes. Certains critères additionnels sont propres à chacune des étiologies. Ainsi, en cas de cirrhose alcoolique, la transplantation n’est envisagée qu’au terme d’une période d’abstinence d’au moins six mois, période minimale indispensable pour s’assurer qu’il n’y a pas eu d’amélioration spontanée. En cas de cirrhose en rapport avec une hépatite virale B, l’absence de réplication virale, qu’elle soit spontanée ou induite par un traitement antiviral, est un préalable indispensable à la transplantation.
Les affections primitives des voies biliaires, cirrhose biliaire primitive et cholangite sclérosante primitive, sont presque toujours associées à une cirrhose secondaire au stade où une transplantation est envisagée. Les indications de la transplantation sont alors comparables à celles des cirrhoses en général. Cependant, indépendamment de ces complications, une bilirubinémie supérieure à 150 µmol/l pendant plusieurs semaines et, en cas de cholangite sclérosante primitive, des épisodes répétés d’angiocholite justifient à eux seuls une transplantation. La fréquence respective des différentes indications de transplantation est représentée sur la Figure 1.
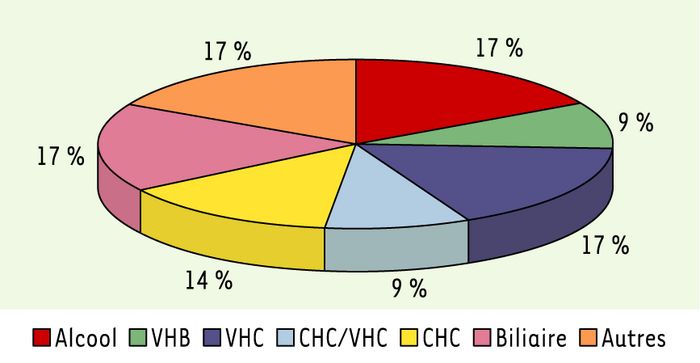
Figure 1
Répartition des indications de transplantation dans le service d’hépatologie de l’hôpital Beaujon entre 1995 et 2001.
Alcool : cirrhose alcoolique ; VHB : cirrhose en rapport avec une infection par le virus de l’hépatite B ; VHC : cirrhose en rapport avec une infection par le virus de l’hépatite C ; CHC : carcinome hépatocellulaire ; CHC/VHC, carcinome hépatocellulaire développé sur une cirrhose d’étiologie virale C ; biliaire : maladie des voies biliaires ; autres : autres affections chroniques du foie.
Tumeurs du foie
Le carcinome hépatocellulaire (CHC), tumeur primitive du foie la plus fréquente, est dans la plupart des cas associé à une cirrhose sous-jacente. La transplantation permet de traiter à la fois le CHC et la cirrhose. Toutefois, elle ne peut être envisagée que pour des tumeurs de petite taille (un nodule unique de moins de 5 cm de diamètre ou deux ou trois nodules de moins de 3 cm) [1]. En effet, même en l’absence de localisation extra-hépatique décelable, les tumeurs plus volumineuses récidivent fréquemment. La récidive est probablement liée à la présence de cellules tumorales circulantes [2]. Chez les malades ayant une tumeur de petite taille et une cirrhose compensée, la résection chirurgicale est une alternative à la transplantation. Cependant, la résection laisse en place un foie cirrhotique et le taux de récidive à cinq ans atteint 80 % environ [3]. Les données les plus récentes suggèrent que les résultats de la transplantation sont supérieurs, avec une survie sans récidive aux alentours de 70 % à cinq ans [4].
En dehors de tumeurs rares dont la progression est particulièrement lente, comme les tumeurs neuro-endocrines, les autres tumeurs primitives ou secondaires du foie représentent en principe une contre-indication à la transplantation en raison d’un risque élevé de récidive précoce.
Insuffisances hépatiques aiguës
Chez la plupart des malades, les insuffisances hépatiques aiguës se corrigent rapidement et sans séquelles du fait de la régénération hépatique. Cependant, chez certains malades, la progression ou la persistance de l’insuffisance hépatique conduit à la constitution d’un oedème cérébral qui peut entraîner le décès en quelques heures ou quelques jours. Dans cette situation, une transplantation doit être réalisée en urgence, ce qui justifie une procédure d’attribution prioritaire des greffons. En règle générale, on prend la décision de transplantation lorsqu’il existe à la fois une encéphalopathie sévère (confusion ou coma) et une diminution marquée des facteurs de coagulation (facteur V inférieur à 20 % chez des sujets de moins de 30 ans ou inférieur à 30 % chez des sujets de plus de 30 ans) [5]. Les principales causes d’insuffisance hépatique aiguë conduisant à la transplantation sont les hépatites virales aiguës B, les hépatites médicamenteuses et certaines hépatites de cause indéterminée.
Contre-indications à la transplantation
Ces contre-indications peuvent être en rapport avec la maladie hépatique elle-même, lorsque le risque de récidive de la maladie initiale compromet la survie à quelques mois, ou avec des affections extra-hépatiques concomitantes qui représentent un risque opératoire majeur (insuffisance cardiaque ou insuffisance respiratoire chronique). Les progrès réalisés dans le domaine des traitements anti-rétroviraux font que l’infection par le VIH, lorsqu’elle est contrôlée, ne constitue plus, à elle seule, une contre-indication formelle à la transplantation, à condition qu’il n’y ait pas de virémie détectable, que le taux de lymphocytes CD4+ soit supérieur à 200/mm3 et qu’il n’y ait pas eu d’infection par des agents opportunistes [6, 7].
Techniques de transplantation hépatique
La transplantation orthotopique totale, technique la plus courante, consiste à transplanter un greffon entier, prélevé chez un sujet en état de mort cérébrale (donneur cadavérique) à la place du foie natif. Au cours des dernières années, le manque de donneurs a conduit à développer des techniques alternatives : le partage du greffon cadavérique pour deux receveurs (split) et la transplantation par donneur vivant.
La transplantation par donneur vivant est fondée sur les quatre principes suivants : chez la plupart des individus, le foie peut être séparé chirurgicalement en deux parties autonomes, droite et gauche ; chez un individu normal, on peut réséquer une partie importante du parenchyme hépatique (jusqu’aux deux tiers environ), la partie restante se régénérant rapidement ; lorsqu’on transplante un greffon partiel de petite taille, celui-ci se régénère pour atteindre une taille proche de celle d’un greffon complet ; enfin, des équipes expérimentées peuvent réaliser une hépatectomie chez un sujet sain avec une morbidité faible et une mortalité inférieure à 1 %. Paradoxalement, le fait que le donneur soit génétiquement apparenté ne semble pas modifier l’incidence du rejet. Globalement, les résultats pour le receveur sont comparables à ceux de la transplantation par donneur en état de mort cérébrale. Toutefois, il s’agit d’une intervention chirurgicale lourde pour le donneur, avec un taux de complications sévères de l’ordre de 15 % à 20 % [8].
Par analogie avec la transplantation par donneur vivant, la technique du foie partagé (ou split) consiste à séparer le foie d’un donneur cadavérique en deux parties autonomes [9]. Cette technique nécessite de réaliser les deux transplantations hépatiques en même temps. En raison de ces difficultés, les greffons ne peuvent être partagés que dans moins de 25 % des cas.
Rejet et traitement immunosuppresseur
Les différents types de rejet
Le rejet aigu, transitoire, est le plus fréquent. Malgré le traitement immunosuppresseur préventif, il s’observe dans 20 % à 25 % des cas, principalement au cours des deux à trois premières semaines [10]. En l’absence de tests diagnostiques non invasifs fiables, le diagnostic repose sur la biopsie du greffon. Chez plus de 90 % des malades, le rejet aigu peut être traité efficacement par des bolus de corticoïdes et/ou une augmentation transitoire de l’immunosuppression de fond [11]. Il est important de noter que la survenue d’un épisode de rejet aigu n’a pas d’influence délétère sur le fonctionnement ultérieur du greffon [12].
Le rejet chronique, plus rare (moins de 5 % des patients), est caractérisé par une disparition progressive des canaux biliaires intra-hépatiques de petite taille (ductopénie) et une artérite diffuse. Lorsqu’il est installé, ce rejet reste peu sensible à l’augmentation de l’immunosuppression et s’accompagne à terme d’une perte fonctionnelle du greffon [13].
Traitement immunosuppresseur
En dehors de cas exceptionnels, un traitement immunosuppresseur permanent est nécessaire pour prévenir le rejet. Cependant, les doses d’immunosuppresseurs peuvent être diminuées, rapidement au cours des premières semaines, puis plus lentement ensuite. Dans les premières semaines, on utilise des associations d’immunosuppresseurs (induction possible par des anticorps antirécepteurs de l’interleukine-2, corticoïdes, anticalcineurines, antiprolifératifs) pour obtenir un niveau élevé d’immunosuppression avec des doses réduites de chacun des agents et peu d’effets secondaires. Les corticoïdes, responsables de nombreux effets secondaires, sont interrompus dans les quatre premiers mois.
À distance de la transplantation, les anti-calcineurines (ciclosporine et tacrolimus ou FK506) sont les immunosuppresseurs de base. Dans la majorité des cas, ils sont suffisants en monothérapie pour prévenir efficacement le rejet. Cependant, leurs effets secondaires peuvent conduire à en limiter les doses, ce qui justifie, en compensation, de les associer à un agent antiprolifératif tel que le mycophénolate mofétil [14]. Éventuellement, on peut remplacer les anticalcineurines par de la rapamycine, seule ou en association avec le mycophénolate mofétil. D’autres agents immunosuppresseurs, tels que le FTY720 ou le FK778, ayant des mécanismes d’action différents de ceux des anticalcineurines, sont en cours de développement.
Facteurs limitant les résultats de la transplantation
Les résultats de la transplantation hépatique sont limités par les complications péri-opératoires et, plus à distance, par des complications chirurgicales, la récidive de la maladie initiale, le rejet chronique, les effets secondaires des immunosuppresseurs et les complications liées à l’état d’immunodépression. Certaines de ces affections peuvent éventuellement être corrigées par une retransplantation.
Complications péri-opératoires et chirurgicales
La mortalité péri-opératoire reste de l’ordre de 5 % à 10 %. Elle est principalement liée à des infections bactériennes ou fongiques. Parmi les complications chirurgicales, les thromboses de l’artère hépatique sont les plus graves. Elles s’observent chez 5 % des malades, environ, et ont pour conséquence une ischémie puis une nécrose plus ou mois étendue des voies biliaires (dont la vascularisation est exclusivement artérielle) [15]. Les complications biliaires sont plus fréquentes (10 % à 20 % environ), mais habituellement moins graves. Il s’agit principalement de sténoses anastomotiques qui peuvent être traitées par voie endoscopique ou par réparation chirurgicale [16].
Récidive de la maladie initiale
La récidive de l’hépatite chronique virale C sur le greffon est presque constante. On estime que 10 % à 30 % des malades ont à nouveau une cirrhose cinq ans après la transplantation [17]. Toutefois, la progression de l’hépatite est très variable d’un sujet à l’autre. Les malades infectés par des virus de génotype 1b (le plus fréquent dans les populations occidentales) semblent avoir une récidive plus agressive. De même, les récidives sont d’autant plus sévères que le donneur est âgé [18]. L’efficacité des traitements antiviraux est plus faible que chez les malades non immunodéprimés. Cependant, les résultats préliminaires concernant l’association d’interféron pégylé et de ribavirine sont encourageants [19].
En cas d’hépatite chronique virale B, la récidive est plus rare, mais progresse beaucoup plus rapidement. L’administration conjointe d’immunoglobulines spécifiques anti-HBs et d’un antiviral (lamivudine) a permis, au cours des dernières années, de réduire l’incidence des récidives aux alentours de 10 % à 15 %, au lieu de 30 % avec les immunoglobulines anti-HBs seules [20, 21]. Cependant, l’administration prolongée de lamivudine est limitée par l’apparition fréquente (jusqu’à 30 % par an) de souches de virus résistants. L’adéfovir semble régulièrement efficace sur ces mutants.
En cas de cirrhose alcoolique, malgré l’application des critères de sélection, environ 50 % des malades reprennent une consommation d’alcool après la transplantation [22]. Cependant, l’expérience montre que la majorité des malades, qui avant la transplantation avaient une consommation excessive d’alcool, parviennent à réduire celle-ci après l’intervention. Globalement, la survie est comparable à celle des malades transplantés pour une cirrhose non alcoolique, au moins dans les cinq à dix premières années.
Pour la cirrhose biliaire primitive et la cholangite sclérosante primitive, la récidive s’observe respectivement dans 10 % à 15 % et 20 % à 25 % des cas. Elle est relativement insensible aux traitements immunosuppresseurs et peut nécessiter une retransplantation.
En cas de CHC, le risque de récidive augmente avec la taille et le nombre des nodules. Pour les malades ayant des tumeurs de petite taille, le taux de récidive à cinq ans se situe aux alentours de 10 % à 20 %. Les récidives sont souvent multifocales et rapidement progressives.
Effets secondaires des agents immunosuppresseurs
Les principaux effets secondaires des agents immunosuppresseurs sont résumés dans le Tableau I. Il est important de noter que certains de ces effets (tremblements et hirsutisme) ne font que réduire la qualité de vie alors que d’autres, comme les complications cardiovasculaires, contribuent notablement à réduire l’espérance de vie [23, 24].
Tableau I
Principaux effets secondaires des agents immunosuppresseurs.
Complications néoplasiques liées à l’état d’immunodépression
Les traitements immunosuppresseurs augmentent le risque de développer un cancer de novo, quel qu’en soit le type. Certains cancers tels que les lymphomes, le sarcome de Kaposi ou les cancers cutanés sont particulièrement fréquents. Globalement, le risque de cancer de novo se situe aux alentours de 20 % à 10 ans et 50 % à 15 ans.
Complications infectieuses liées à l’état d’immunodépression
Les complications infectieuses graves, bactériennes et fongiques, se manifestent essentiellement pendant la période post-opératoire précoce. Malgré le traitement immunosuppresseur, les infections sévères sont rares à distance de la transplantation, y compris les infections par des agents opportunistes. Les traitements antiviraux (gancyclovir, acyclovir et valacyclovir) ont fortement diminué l’incidence des infections par le cytomégalovirus.
Résultats
Espérance de vie
Quelle que soit l’indication de la transplantation, la courbe de survie est marquée par un infléchissement initial correspondant à la mortalité post-opératoire précoce. Au-delà des trois à six premiers mois, la courbe de survie tend à devenir horizontale. À cinq ans, la survie des malades transplantés pour une cirrhose décompensée est de l’ordre de 70 % à 80 %. La survie des malades transplantés pour un CHC est un peu plus faible, de l’ordre de 60 % à 70 % à cinq ans. La différence est liée aux récidives tumorales, responsables d’une décroissance plus tardive de la courbe de survie. La survie des malades transplantés pour une insuffisance hépatique aiguë est de l’ordre de 60 % à cinq ans. Dans ce cas, la mortalité post-opératoire précoce est plus élevée (Figure 2).
Figure 2
Espérance de vie à trois ans après transplantation hépatique entre 1995 et 2001 dans le service d’hépatologie de l’hôpital Beaujon.
Cirrhoses sans carcinome hépato-cellulaire (ligne rouge) : 72 % ; carcinome hépatocellulaire (ligne verte) : 62 % ; hépatites fulminantes et subfulminantes (ligne pointillée bleue) : 65 %.
Qualité de vie
Les malades transplantés pour une cirrhose retrouvent dans la majorité des cas une autonomie complète dans la vie quotidienne. Les contraintes liées au traitement immunosuppresseur et à la surveillance médicale sont relativement faibles [25]. Malgré cela, seule une minorité des malades peut reprendre une activité professionnelle en raison d’une interruption prolongée de celle-ci avant la transplantation et de la difficulté à trouver un emploi adapté.
Conclusions et perspectives
La transplantation hépatique, bien qu’elle représente une intervention chirurgicale lourde, améliore notablement le pronostic des cirrhoses décompensées, des CHC de petite taille et des formes les plus graves d’insuffisance hépatique aiguë. Elle permet, dans la majorité des cas, la restauration d’une qualité de vie proche de la normale avec des contraintes médicales réduites. Le principal facteur limitant est l’accès à la transplantation, en raison du déséquilibre entre le nombre de candidats potentiels et le nombre de donneurs. Ces résultats justifient les efforts pour tenter d’augmenter le taux de prélèvement chez les sujets en état de mort cérébrale et d’optimiser l’attribution des greffons aux malades qui ont le plus de chances d’en tirer un bénéfice. Des recherches doivent également être consacrées au développement de traitements immunosuppresseurs ayant moins d’effets secondaires à long terme.
Parties annexes
Références
- 1. Mazzaferro V, Regalia E, Doci R, et al. Liver transplantation for the treatment of small hepatocellular carcinomas in patients with cirrhosis. N Engl J Med 1996 ; 334 : 693-9.
- 2. Kar S, Carr BI. Detection of liver cells in peripheral blood of patients with advanced stage hepatocellular carcinoma. Hepatology 1995 ; 21 : 403-7.
- 3. Belghiti J, Panis Y, Farges O, et al. Intrahepatic recurrence after resection of hepatocellular carcinoma complicating cirrhosis. Ann Surg 1991 ; 214 : 114-7.
- 4. Hemming AW, Cattral MS, Reed AI, et al. Liver transplantation for hepatocellular carcinoma. Ann Surg 2001 ; 223 : 652-9.
- 5. Bernuau J, Rueff B, Benhamou JP. Fulminant and subfulminant liver failure : definitions and causes. Semin Liver Dis 1986 ; 6 : 97-106.
- 6. Gow PJ, Pillay D, Mutimer D. Solid organ transplantation in patients with HIV infection. Transplantation 2001 ; 72 : 177-81.
- 7. Prachalias AA, Pozniak A, Taylor C, et al. Liver transplantation in adults coinfected with HIV. Transplantation 2001 ; 72 : 1684-8.
- 8. Trotter JF, Talamantes M, McClure M, et al. Right hepatic lobe donation for living donor liver transplantation : impact on donor quality of life. Liver Transpl 2001 ; 7 : 485-93.
- 9. Toso C, Ris F, Mentha G, et al. Potential impact of in situ liver splitting on the number of available grafts. Transplantation 2002 ; 74 : 222-6.
- 10. O’grady JG, Burroughs A, Hardy P, et al. Tacrolimus versus microemulsified ciclosporin in liver transplantation : the TMC randomised controlled trial. Lancet 2002 ; 360 : 1119-25.
- 11. Boillot O, Viale JP, Gratadour P, et al. Reversal of early acute rejection with increased doses of tacrolimus in liver transplantation : a pilot study. Transplantation 1998 ; 66 : 1182-5.
- 12. Wiesner RH, Demetris AJ, Belle SH, et al. Acute hepatic allograft rejection : incidence, risk factors and impact on outcome. Hepatology 1998 ; 28 : 638-45.
- 13. Shirwan H. Chronic allograft rejection. Transplantation 1999 ; 68 : 715-26.
- 14. Schlitt HJ, Barkmann A, Boker KHW, et al. Replacement of calcineurin inhibitors with mycophenolate mofetil in liver transplant patients with renal dysfunction : a randomised controlled study. Lancet 2001 ; 357 : 587-91.
- 15. Denys AL, Qanadli SD, Durand F, et al. Feasibility and effectiveness of using coronary stents in the treatment of hepatic artery stenoses after orthotopic liver transplantation : preliminary report. Am J Roentgenol 2002 ; 178 : 1175-9.
- 16. Sawyer SG, Punch JD. Incidence and management of biliary complications after 291 following the introduction of transcystic stenting. Transplantation 1998 ; 66 : 1201-7.
- 17. Berenguer M, Ferrell L, Watson J, et al. HCV-related fibrosis progression following liver transplantation : increase in recent years. J Hepatol 2000 ; 32 : 673-84.
- 18. Wali M, Harrison RF, Gow PJ, Mutimer D. Advancing donor liver age and rapid fibrosis progression following transplantation for hepatitis C. Gut 2002 ; 51 : 248-52.
- 19. Lavezzo B, Franchello A, Smedile A, et al. Treatment of recurrent hepatitis C in liver transplants : efficacy of a six versus twelve month course of interferon alfa 2b with ribavirin. J Hepatol 2002 ; 37 : 247-52.
- 20. Lo CM, Fan ST, Liu CL, et al. Prophylaxis and treatment of recurrent hepatitis B virus infection after liver transplantation. Transplantation 2003 ; 75 : S41-4.
- 21. Fontana RJ, Hann HW, Wright T, et al. A multicenter study of lamivudine treatment of 33 patients with hepatitis B after liver transplantation. Liver Transpl 2001 ; 7 : 504-10.
- 22. Gerhardt TC, Goldstein RM, Urschel HC, et al. Alcohol use following liver transplantation for alcoholic cirrhosis. Transplantation 1996 ; 62 : 1060-3.
- 23. Selzner N, Durand F, Bernuau J, et al. Conversion from cyclosporine to FK506 in adult liver transplant recipients : a combined north american and european experience. Transplantation 2001 ; 72 : 1061-5.
- 24. Ojo AO, Held PJ, Port FK, et al. Chronic renal failure after transplantation of a nonrenal organ. N Engl J Med 2003 ; 349 : 931-40.
- 25. Dew MA, Switzer GE, Goycoolea JM, et al. Does transplantation produce quality of life benefits ? Transplantation 1997 ; 64 : 1261-73.
Liste des figures
Figure 1
Répartition des indications de transplantation dans le service d’hépatologie de l’hôpital Beaujon entre 1995 et 2001.
Alcool : cirrhose alcoolique ; VHB : cirrhose en rapport avec une infection par le virus de l’hépatite B ; VHC : cirrhose en rapport avec une infection par le virus de l’hépatite C ; CHC : carcinome hépatocellulaire ; CHC/VHC, carcinome hépatocellulaire développé sur une cirrhose d’étiologie virale C ; biliaire : maladie des voies biliaires ; autres : autres affections chroniques du foie.
Figure 2
Espérance de vie à trois ans après transplantation hépatique entre 1995 et 2001 dans le service d’hépatologie de l’hôpital Beaujon.
Liste des tableaux
Tableau I
Principaux effets secondaires des agents immunosuppresseurs.