Abstracts
Résumé
Le gène hairless (hr) des mammifères code pour une protéine nucléaire impliquée dans le contrôle du renouvellement du follicule pileux. Cette protéine est un cofacteur de récepteurs nucléaires d’hormones qui régulent la transcription de gènes cibles au cours de la différentiation de l’épiderme et du cycle du poil. La protéine Hairless (HR) fait partie de grands complexes multiprotéiques capables de réprimer la transcription, en association avec des facteurs de remodelage de la chromatine comme les histones désacétylases. Chez les mammifères, le locus hairless est la cible de nombreuses mutations alléliques dont les effets sont pléiotropiques. Ces altérations entraînent l’apparition d’un phénotype cutané complexe, caractérisé par la perte progressive et irréversible d’un pelage d’apparence normale au cours des premières semaines de vie post-natale. L’analyse de la littérature sur le gène hairless chez la souris et chez l’homme permet d’attribuer des différences morphologiques spécifiques à chaque mutant, aussi bien au niveau de l’épiderme et du follicule pileux que dans d’autres tissus où le gène est exprimé au cours du développement. Ces résultats suggèrent que l’intégrité du gène hairless est requise pour le déroulement correct de la morphogenèse d’organes aussi différents que l’épiderme, l’oreille interne, l’ovaire ou le thymus. Le gène hairless semble ainsi faire partie de circuits et de cascades d’interactions géniques dont le contrôle moléculaire est fondamentalement inconnu. La variété des phénotypes alléliques souligne l’importance de l’analyse moléculaire du locus hairless pour identifier les altérations géniques impliquées dans les différentes mutations détectées. Les recherches concernant la mutation hairless ont été particulièrement dynamiques pendant les dernières années, depuis que l’homologue de ce gène a pu être mis en évidence chez l’homme. Cependant, un bon nombre de questions reste en suspens, notamment quant au site exact d’activité du gène hairless au sein des nombreuses populations cellulaires du follicule pileux, son rôle précis au cours de la morphogenèse, sa localisation au sein des voies de signalisation, ainsi que l’identité des partenaires et des cibles de la protéine Hairless.
Summary
The hairless gene in mammals encodes a nuclear factor that is highly expressed in skin and appears to control hair follicle integrity and cycling. In the absence of a normal and functional Hairless (Hr) protein, the hair bulb undergoes premature apoptosis during the first catagen stage of the hair cycle. The most striking effects of the mutation are loss of hair follicles and formation of epidermal utricles and dermal cysts. The hairless gene expression appears to be widespread and temporally regulated. The gene is strongly expressed in different compartments of the brain. Hairless mRNAs were detected in cartilage, gonads, thymus and colon. In addition to alopecia, hairless mice strains show subtle defects in the development and differentiation of various tissues and organs. The Hr protein is localised in cell nuclei and functions as a transcriptional regulator. Although its role has not been resolved in molecular terms, it was demonstrated that Hr is able to interact with multiple nuclear hormone receptors. Hr seems to be a part of a large multiprotein complex capable to repress transcription by its association to chromatin remodelling factors such as histone deacetylases. Recent experimental data suggest that Hr might be involved in Hox gene regulation, cell adhesion modulation and progenitor cells identity. At least in the skin, but probably in other organs, the Hr repressor seems to be responsible for the timing of epithelial cells differentiation.
Article body
La perte d’un pelage d’apparence normale vers la fin de la troisième semaine de vie post-natale est le caractère marquant de la souris hairless. Des mutants spontanés hairless sont observés et étudiés depuis plus d’un siècle, et des lignées de souris hairless ont été systématiquement élevées et maintenues en laboratoire dans les années 20 ; depuis cette période, un certain nombre de variants alléliques ont été identifiés [1]. La souris hairless a été un excellent modèle en dermatologie, pour étudier les différents types d’alopécie et évaluer l’activité et l’absorption cutanée des médicaments, ainsi que dans l’analyse de la formation des rides. L’utilisation de ces mutants permet d’explorer les effets protecteurs des anti-oxydants sur la peau et les étapes successives de la progression tumorale induite par les agents chimiques ou les rayons UV, ainsi que d’étudier divers aspects de la physiologie de la peau et du processus de vieillissement [2-4].
Cependant, les fondements moléculaires et cellulaires de cette mutation, l’identification du gène hairless lui-même, ainsi que l’analyse de son rôle biologique n’ont été abordés que très récemment. En effet, les recherches sur les différents variants alléliques ne se sont dynamisées que ces dernières années, depuis que le gène hairless a été cloné chez la souris, et surtout que l’homologue de ce gène a été identifié chez l’homme [5, 6].
Le locus hairless des mammifères
Le gène hairless (hr) est remarquablement conservé chez les mammifères. L’homologie des séquences codantes chez la souris, le rat, l’homme, le singe, le chien, le porc et le mouton varie entre 70 % et 80 %, et atteint 82 % dans les cas de la souris et de l’homme [6] ; cette conservation témoigne d’un rôle essentiel chez les mammifères, et qui leur est spécifique : de fait, des recherches menées in silico n’ont pas permis d’identifier des orthologues de hairless dans divers phylums majeurs de vertébrés ou d’invertébrés. Il est donc possible que le gène hairless n’existe que chez les mammifères, et que sa fonction soit intimement liée à l’apparition du pelage au cours de l’évolution.
Le gène hairless est situé sur le chromosome 14 chez la souris et sur le chromosome 8 chez l’espèce humaine. Chez l’ensemble des mammifères analysés, ce gène s’étend sur une séquence génomique d’environ 20 kb. Il est organisé en 19 exons et sa transcription produit un ARNm d’environ 5 kb [7]. Bien que de nombreux variants alléliques aient été identifiés chez la souris, la nature précise des altérations affectant le gène hairless n’a pu être identifiée que dans quelques cas sur une douzaine de lignées mutantes obtenues et décrites à ce jour (Figure 1) : le mutant hr original comporte l’insertion d’un provirus au niveau de l’intron 6 [8] ; la mutation hrrhY consisterait en une insertion de 13 pb dans l’exon 16 [9] ; la mutation hrrhTgN5053Mm serait due à l’insertion d’un transgène au niveau du locus hairless [10] ; les souris bald Mill Hill présentent, quant à elles, une délétion de 296 pb à l’extrémité 3’ de l’exon 19 du gène [11] ; enfin, des mutations faux-sens ont été identifiées au niveau des exons 12 et 4 chez les souris hrrhsl, hrrhChr et hr rh8J [12-14].
Figure 1
Le gène hairless chez la souris et les différentes mutations identifiées.
Le gène hairless est constitué de 19 exons et s’étend sur une longueur génomique d’environ 20 kb. À ce jour, une douzaine de lignées mutantes ont été répertoriées, mais l’altération génique précise n’a été identifiée que dans les cas présentés sur cette figure.
Chez l’homme, l’atrichose généralisée (absence totale de poils et de cheveux) est une pathologie à hérédité autosomique récessive. Tout comme chez les souris, un certain nombre de mutations du gène hairless humain ont été mises en évidence [15] : dans la plupart des cas, ces anomalies consistent en altérations ponctuelles, délétions ou insertions. Le désordre, répertorié sous les termes d’alopécie universelle congénitale (OMIM#203655) ou atrichose à papules (OMIM#209500), reste extrêmement rare chez l’homme [16] : les individus affectés proviennent généralement de mariages consanguins, et une dizaine de familles, avec à peine une centaine d’individus à alopécie totale, ont été décrits dans le monde.
Expression du gène hairless au cours du développement et dans le cycle pilaire
Chez la souris, le gène hairless s’exprime dès le jour E11,5 dans l’épiderme embryonnaire. Son activité est notamment détectée au niveau des placodes épidermiques, qui constituent les primordia des vibrisses et des follicules pileux. D’autres zones d’expression apparaissent, à des stades plus tardifs (E14,5-E16,5), au niveau du cerveau, de la rétine et des nerfs optiques, ainsi que dans les poumons et dans les épithéliums de la langue et du côlon [17]. Chez les nouveau-nés, l’ARNm est présent d’abord dans les couches suprabasales de l’épiderme et au centre de la partie distale du bourgeon du poil. Ensuite, deux nouvelles zones d’expression apparaissent au niveau de la matrice du poil en formation et dans la gaine interne (GI) du follicule pileux [18].
Au cours des trois phases du cycle du poil (anagène, phase de croissance ; catagène, phase de régression ; et télogène, phase de repos) ((→) m/s 2006, n° 2 p. 138), les profils d’expression varient de façon dymanique : au fur et à mesure de la progression en phase anagène, hr est exprimé dans une fine couche cellulaire de la gaine externe (GE), puis son expression se concentre au niveau des cellules de la matrice du poil ; en phase catagène, une nouvelle zone d’expression est détectée au niveau de la GE qui entoure l’extrémité proximale de la tige du poil ; en fin de régression pilaire et au stade télogène, le gène hairless s’exprime au niveau de quelques cellules appartenant au cordon de cellules épithéliales qui relie la papille dermique au reste du follicule [18]. Ces patrons d’expression suggèrent que le gène hairless serait un facteur clé dans la coordination de processus cellulaires tels que la formation de la racine du poil, le maintien de l’intégrité de la papille dermique ou la désintégration des gaines épithéliales du poil au cours du stade catagène. L’expression du gène hairless est donc finement régulée dans le temps et dans l’espace, et la majorité des structures affectées chez les mutants sont des sites d’une forte activité de transcription de ce gène.
Phénotype majeur et effets pléiotropiques des mutations du locus hairless
Follicule pileux
L’énigme fondamentale des mutants hairless, qui fascine les chercheurs depuis plus d’un siècle, est que le follicule pileux des mutants homozygotes, après avoir donné un premier poil d’apparence normale, soudain se désintègre en laissant derrière lui deux malformations typiques : des utricules au niveau de l’épiderme et des kystes dermiques en profondeur. La première caractéristique observable chez les mutants est un élargissement de la partie supérieure des follicules pileux. Cette dilatation progresse dans le sens proximal et la cavité folliculaire se remplit de matériel corné. L’examen détaillé de l’épiderme mutant indique que la GE et la GI du follicule perdent leur intégrité, et que l’organisation des couches cellulaires est gravement perturbée [3] : les gaines se désagrègent, et la tige du poil perd son ancrage. Les utricules, ou petites poches épithéliales remplies de matériel corné et de kératinocytes en dégénérescence, peuvent communiquer ou non avec les kystes profonds [11] ; le nombre et le volume de ces kystes augmentent avec l’âge, et vont donner chez la souris des replis et des rides cutanés typiques pour les variants « rhinocéros » (Figure 2).
Figure 2
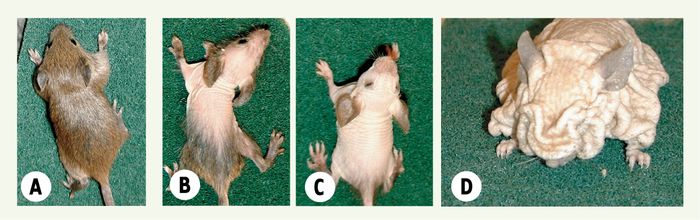
Phénotype des mutants hairless.
A. La première pousse de poils est d’apparence normale. B, C. Deux semaines après la naissance, les mutants développent une alopécie de l’avant vers l’arrière de leurs corps (B) qui aboutit à la perte totale et irréversible du pelage (C). D. Avec l’âge, la peau des animaux mutants a tendance à s’épaissir et à former des replis cutanés, particulièrement prononcés au niveau du museau.
Chez l’homme, cette anomalie conduit à une perte des poils, des cheveux, des cils et des sourcils dans les premiers mois après la naissance. Les patients peuvent, rarement, garder leurs cils et sourcils, en développant avec l’âge des granulomes cutanés au niveau des kystes dermiques [19, 20]. Aussi bien chez l’homme que chez la souris, le défaut majeur évident chez les mutants est l’incapacité du follicule pileux à initier son propre renouvellement cyclique. Or la mise en place, le maintien et le cycle des follicules pileux résultent d’un ensemble de processus complexes faisant intervenir, à chaque étape, de profonds remaniements cellulaires finement régulés ; l’analyse par des approches de haut débit a révélé plus d’une centaine de protéines structurales et régulatrices localisées de façon spécifique dans les compartiments épidermiques et la papille folliculaire mésenchymateuse [21].
Organes affectés chez la souris
De nombreuses études font état d’anomalies au niveau du système immunitaire chez les mutants hairless : chez des souris hairless âgées de deux mois, les stades tardifs de la différenciation thymocytaire sont sévèrement affectés ; chez les souris Yurlovo, dont l’espérance de vie ne dépasse pas six mois, une involution et une disparition du thymus entre le troisième et le sixième mois ont été observées [9] ; chez les mutants rhino-j, on constate des défauts du système immunitaire, en particulier dans les fonctions des cellules T-auxiliaires et des macrophages, souvent accompagnés d’une atrophie de la région corticale du thymus dès le troisième mois après la naissance [22]. En revanche, les souris hairless bald Mill Hill ne présentent aucune anomalie de la différenciation ou de la maturation des thymocytes [11].
Si les mâles hairless et rhino sont apparemment féconds, les mutants rhino Yurlovo perdent leur capacité de reproduction vers l’âge de 4-5 mois, en même temps qu’ils présentent une diminution du poids de leurs testicules [9]. En règle générale, les femelles qui portent des mutations du gène hairless présentent des anomalies de la reproduction mal élucidées, qui vont souvent jusqu’à l’infertilité complète et définitive : ces femelles sont caractérisées par des troubles du fonctionnement des glandes mammaires, ou par des anomalies pathologiques de leur cycle ovarien et du cycle de l’épithélium utérin. De plus, les femelles mutantes présentent des anomalies dans leur comportement maternel : elles ne s’occupent pas de leurs petits, et sont incapables de les nourrir ou de les élever [23].
Au niveau du système nerveux central, la rétine, le cervelet et l’oreille interne sont souvent affectées chez les souris rhino : il a ainsi été établi que la couche plexiforme interne et la couche ganglionnaire de la rétine sont fortement réduites chez des individus homozygotes ; l’analyse de la structure du cerveau chez les mutants rhino-j indique que le gène hairless est impliqué dans la maturation et le maintien de la différenciation du cortex du cervelet [24] ; chez les mutants adultes, la taille, la morphologie et l’immunoréactivité pour des marqueurs neuronaux (NFP et CB) des cellules de Purkinje sont modifiées, la mutation semblant être liée à une accélération du vieillissement du cervelet [24] ; enfin, au niveau de l’oreille interne, une perte de grands neurones ganglionnaires de la cochlée, accompagnée par des anomalies de l’épithélium sensoriel, a souvent été observée chez les mutants. En revanche, une hyperprolifération de l’épithélium du colon est notée chez les souris hrrh [17] : l’anomalie semble liée à une augmentation du nombre de villosités intestinales et du diamètre de la muqueuse musculaire de l’intestin des mutants.
Cette variété de phénotypes subtils, qui accompagnent la perte du poil, illustre les fonctions multiples du gène hairless au cours du développement, un gène dont la régulation, les partenaires et les cibles sont encore bien méconnus.
Hairless, une protéine au centre de plusieurs voies de signalisation
Un corépresseur des récepteurs nucléaires d’hormones
Chez la souris, la protéine Hairless (HR) est constituée de 1 182 acides aminés, pour une masse moléculaire de 127 kDa (Figure 3). La structure primaire de la protéine ne présente aucune homologie évidente avec des protéines aux fonctions connues, ce qui aurait permis de prédire son rôle.
Figure 3
Structure de la protéine Hairless.
Chez la souris, la protéine Hairless (HR) est composée de 1 182 acides aminés et présente une masse moléculaire de 127 kDa. Morphologiquement, la protéine Hairless ne possède pas de motifs structuraux distinctifs, à l’exception d’une séquence putative à doigt de zinc entre les acides aminés 590 et 625 (ZF). La protéine Hairless se localise dans le noyau, grâce à une séquence signal de localisation nucléaire bipartite (NLS, nuclear localisation signal), située entre les acides aminés 409 et 427. Des domaines d’interaction avec des récepteurs nucléaires d’hormones ont été identifiés dans la protéine Hairless de rat qui présente 95 % d'identité avec celle de la souris : les domaines d’interaction avec les récepteurs nucléaires de l’hormone thyroïdienne (TR) sont situés entre les acides aminés 750 et 864 (TR-ID1) et les acides aminés 980 et 1 084 (TR-ID2) ; la région située entre les acides aminés 750 et 864 comprend également le domaine d’interaction avec le récepteur de la vitamine D (VDR-ID), ainsi que les motifs LXXLL capables d’interagir avec le récepteur α-orphelin des rétinoïdes (RORα-ID). La protéine Hairless serait un corépresseur ; des analyses fonctionnelles ont révélé l’existence de trois domaines de répression, RD1, RD2, RD3, situés entre les acides aminés 236 et 450, 750 et 864, et 864 et 980, respectivement. La protéine HR est également capable de réguler la voie Wnt en réprimant le gène Wise, un inhibiteur de la voie Wnt.
Morphologiquement, Hairless ne possède pas de motifs structuraux distinctifs, à l’exception d’une séquence putative à doigt de zinc, entre les acides aminés 590 et 625, qui présente une certaine similitude avec les doigts de zinc des facteurs de transcription de la famille GATA ; bien que la fonctionnalité du motif n’ait encore jamais été abordée, sa conservation chez les mammifères souligne son importance au sein de la protéine. De plus, HR adopte une localisation nucléaire grâce une séquence signal de localisation nucléaire bipartite, située entre les acides aminés 409 et 427 ; l’analyse par fractionnement cellulaire confirme cette localisation nucléaire de la protéine HR, qui serait fortement associée à la matrice nucléaire [25].
Les premiers résultats de la dissection des domaines fonctionnels indiquent que les récepteurs nucléaires d’hormones comme les TR (récepteurs de l’hormone thyroïdienne), le VDR (récepteur de la vitamine D) ou les RAR (récepteurs de l’acide rétinoïque) compteraient parmi les partenaires privilégiés de la protéine HR : de fait, le gène hairless semble être une cible de l’hormone thyroïdienne dans le système nerveux central, et la protéine HR interagit directement avec les récepteurs nucléaires de cette hormone. Deux domaines capables d’interagir avec les TR ont été identifiés, entre les acides aminés 750 et 864 (ID1) et 980 et 1 084 (ID2) [26]. La protéine HR se lie également au récepteur nucléaire orphelin ROR-α par l’intermédiaire de deux motifs LXXLL, situés entre les acides aminés 568 et 784 [27, 28]. Enfin, Hr interagirait physiquement avec VDR in vitro comme in vivo, par un domaine compris entre les acides aminés 750 et 864 [29].
Le rôle de HR dans toutes ces interactions serait celui d’un corépresseur : des analyses fonctionnelles récentes ont en effet révélé l’existence de trois domaines de répression au niveau de la protéine HR, RD1, RD2 et RD3, situés entre les acides aminés 236 et 450, 750 et 864, et 864 et 980, respectivement. Cette activité endogène de répression est probablement assurée par l’intermédiaire de facteurs de remodelage de la chromatine : en effet, HR semble être associée de façon sélective à un sous-groupe d’enzymes de remodelage de la chromatine, les histone désacétylases (HDAC) 1, 3 et 5, capables d’imposer une répression de l’activité transcriptionnelle aux éléments régulateurs des gènes cibles [30]. Cela suggère que HR fait partie d’un immense complexe multiprotéique régulant la répression de la transcription, la spécificité cellulaire et tissulaire étant conférée par le choix de partenaires fonctionnels. Cette interprétation se complique toutefois à la lumière de résultats très récents, qui indiquent que la protéine HR normale elle-même pourrait avoir une activité d’histone désacétylase.
Hairless et Hox
Des résultats récents obtenus à partir du croisement de mutants hairless avec des souris transgéniques suggèrent l’existence d’une relation, directe ou indirecte, entre la protéine Hairless et les membres du complexe Hox [11] : chez les mutants bald Mill Hill, l’expression du marqueur transgénique Hoxb4/LacZ au niveau des placodes épidermiques est en effet absente, ou confinée à quelques cellules seulement (Figure 4). Ces données indiquent que le gène hairless pourrait être spécifiquement impliqué dans l’organisation de la placode du follicule pileux, dès les premiers stades de son expression au niveau de l’embryon en développement. Il est possible d’imaginer que la morphogenèse normale du follicule pileux et sa polarité antéro-postérieure ou proximo-distale, qui dépendent du code Hox régional, soit également sous la dépendance de facteurs ou cofacteurs intervenant au niveau de chaque structure embryonnaire. De plus, la surexpression de la protéine HOXB4 dans des cultures primaires de cellules au stade nouveau-né affecte spécifiquement la prolifération des kératinocytes, et altère l’expression des molécules d’adhésion présentes à leur surface [31].
Figure 4
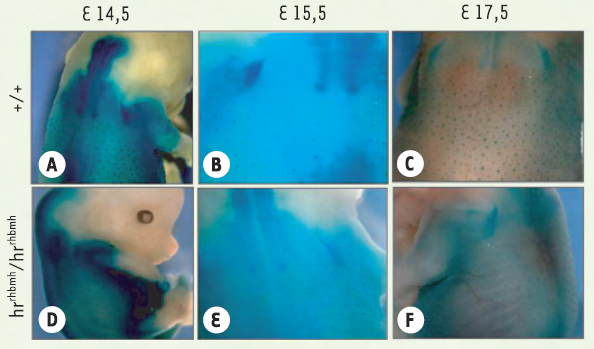
Profil d’expression du transgène Hoxb4/LacZ au cours de l’embryogenèse.
A, B, C. Chez des embryons de type sauvage, le marqueur est fortement exprimé dans les placodes du follicule pileux (A : E14,5 ; B : E15,5 et C : E17,5). D, E, F. On note une disparition de l’expression du transgène chez les mutants hairless aux mêmes stades de développement embryonnaire
Hairless, cellules souches et voie Wnt
Le rôle fonctionnel de Hairless se situe bien dans le contexte de la différenciation des cellules épithéliales. En effet, la régénération continue de l’épiderme et le renouvellement cyclique du follicule pileux dépendent de cellules souches épithéliales localisées dans des niches spécialisées de la gaine externe [32] ; ces cellules souches sont à l’origine de précurseurs multipotents, qui migrent dans les deux sens pour peupler l’épiderme et régénérer les follicules pileux [33], et dont la différenciation dépend de signaux moléculaires sécrétés, comme SHH (sonic-hedgehog), BMP (bone morphoprotein) ou WNT (wingless homolog).
De très récents travaux illustrent le lien entre la destinée des cellules souches et le phénotype mutant, et établissent une association fonctionnelle entre Hairless et la voie Wnt. L’invalidation du gène hairless par recombinaison homologue suggère que l’intégrité de la protéine est nécessaire pour le déroulement correct de la migration des cellules souches, comme cela a été confirmé par le comportement de marqueurs de la différentiation et par l’analyse du transcriptome des kératinocytes des souris invalidées [34]. En ciblant l’expression de la protéine HR de type sauvage dans les précurseurs des kératinocytes, il est possible de corriger le phénotype hairless et de rétablir de façon durable et définitive le cycle du poil chez des individus hr-/-. Cette étude par sauvetage transgénique a, par ailleurs, permis de constater que HR contrôle la signalisation Wnt en réprimant le gène Wise, un inhibiteur bien connu de la voie Wnt [35].
Le gène hairless serait donc responsable de la coordination de l’expression des gènes impliqués dans la prolifération cellulaire, la signalisation et la migration des cellules souches, pour réguler dans le temps et dans l’espace la formation, la différenciation et le cycle du poil.
Conclusions
L’intérêt d’étudier la mutation hairless et ses interactions avec les membres des grandes familles géniques impliquées dans le développement est double. Il est d’une part fondamental, parce que le poil permet d’étudier simultanément plusieurs processus mis en oeuvre au cours de la formation d’un grand nombre de tissus : parmi ces processus figurent les interactions épithélio-mésenchymateuses, le cycle du poil, ainsi que la localisation et le maintien de la pluripotence des cellules souches. D’autre part, une meilleure connaissance des acteurs de la morphogenèse et de la physiologie de la peau apporterait de nombreux espoirs d’application des thérapies cellulaires dans le traitement des alopécies et des anomalies de différenciation des cellules de la couche basale de l’épiderme et du follicule pileux.
Appendices
Remerciements
Les auteurs remercient l’Inserm, la Région Rhône-Alpes et le Ministère de la Recherche pour leur soutien financier.
Références
- 1. Sundberg JP, Price VH, King LE Jr. The “hairless” gene in mouse and man. Arch Dermatol 1999 ; 135 : 718-20.
- 2. Kitazawa M, Ishitsuka Y, Kobayashi M, et al. Protective effects of an antioxidant derived from serine and vitamin B6 on skin photoaging in hairless mice. Photochem Photobiol 2005 ; 81 : 970-4.
- 3. Panteleyev AA, Paus R, Ahmad W, et al. Molecular and functional aspects of the hairless (hr) gene in laboratory rodents and humans. Exp Dermatol 1998 ; 7 : 249-67.
- 4. Dainichi T, Amano S, Matsunaga Y, et al. Chemical peeling by SA-PEG remodels photo-damaged skin : suppressing p53 expression and normalizing keratinocyte differentiation. J Invest Dermatol 2006 ; 126 : 416-21.
- 5. Ahmad W, Faiyaz ul Haque M, Brancolini V, et al. Alopecia universalis associated with a mutation in the human hairless gene. Science 1998 ; 279 : 720-4.
- 6. Cichon S, Anker M, Vogt IR, et al. Cloning, genomic organization, alternative transcripts and mutational analysis of the gene responsible for autosomal recessive universal congenital alopecia. Hum Mol Genet 1998 ; 7 : 1671-9.
- 7. Cachon-Gonzalez MB, Fenner S, Coffin JM, et al. Structure and expression of the hairless gene of mice. Proc Natl Acad Sci USA 1994 ; 91 : 7717-21.
- 8. Stoye JP, Fenner S, Greenoak GE, et al. Role of endogenous retroviruses as mutagens : the hairless mutation of mice. Cell 1988 ; 54 : 383-91.
- 9. Panteleyev AA, Ahmad W, Malashenko AM, et al. Molecular basis for the rhino Yurlovo (hr[rhY]) phenotype : severe skin abnormalities and female reproductive defects associated with an insertion in the hairless gene. Exp Dermatol 1998 ; 7 : 281-8.
- 10. Jones JM, Elder JT, Simin K, et al. Insertional mutation of the hairless locus on mouse chromosome 14. Mamm Genome 1993 ; 4 : 639-43.
- 11. Brancaz MV, Iratni R, Morrison A, et al. A new allele of the mouse hairless gene interferes with Hox/LacZ transgene regulation in hair follicle primordia. Exp Mol Pathol 2004 ; 76 : 173-81.
- 12. Zhang J, Fang S, Wang CY. A novel nonsense mutation and polymorphisms in mouse hairless gene. J Invest Dermatol 2005 ; 124 : 1200-5.
- 13. Ahmad W, Panteleyev AA, Henson-Apollonio V, et al. Molecular basis of a novel rhino (hr(rhChr)) phenotype : a nonsense mutation in the mouse hairless gene. Exp Dermatol 1998 ; 7 : 298-301.
- 14. Ahmad W, Panteleyev AA, Sundberg JP, Christiano AM. Molecular basis for the rhino (hrrh-8J) phenotype : a nonsense mutation in the mouse hairless gene. Genomics 1998 ; 53 : 383-6.
- 15. Bernard BA. Hairless and genetic disorders of hair. Med Sci (Paris) 2002 ; 18 : 276-80.
- 16. Indelman M, Bergman R, Lestringant GG, et al. Compound heterozygosity for mutations in the hairless gene causes atrichia with papular lesions. Br J Dermatol 2003 ; 148 : 553-7.
- 17. Cachon-Gonzalez MB, San-Jose I, Cano A, et al. The hairless gene of the mouse : relationship of phenotypic effects with expression profile and genotype. Dev Dyn 1999 ; 216 : 113-26.
- 18. Panteleyev AA, Paus R, Christiano AM. Patterns of hairless (hr) gene expression in mouse hair follicle morphogenesis and cycling. Am J Pathol 2000 ; 157 : 1071-9.
- 19. Klein I, Bergman R, Indelman M, Sprecher E. A newborn presenting with congenital blistering. Int J Dermatol 2004 ; 43 : 295-7.
- 20. Klein I, Bergman R, Indelman M, Sprecher E. A novel missense mutation affecting the human hairless thyroid receptor interacting domain 2 causes congenital atrichia. J Invest Dermatol 2002 ; 119 : 920-2.
- 21. Botchkarev VA, Kishimoto J. Molecular control of epithelial-mesenchymal interactions during hair follicle cycling. J Invest Dermatol Symp Proc 2003 ; 8 : 46-55.
- 22. San Jose I, Garcia-Suarez O, Hannestad J, et al. The thymus of the hairless rhino-j (hr/rh-j) mice. J Anat 2001 ; 198 : 399-406.
- 23. Sundberg J. The hairless (hr) and rhino (hr rh) mutatons, chromosome 14. In : Sundberg J, ed. Handbook of mouse mutations with skin and hair abnormalities. Boca Raton : CRC Press, 1994 : 291-312.
- 24. Garcia-Atares N, San Jose I, Cabo R, et al. Changes in the cerebellar cortex of hairless Rhino-J mice (hr-rh-j). Neurosci Lett 1998 ; 256 : 13-6.
- 25. Djabali K, Aita VM, Christiano AM. Hairless is translocated to the nucleus via a novel bipartite nuclear localization signal and is associated with the nuclear matrix. J Cell Sci 2001 ; 114 : 367-76.
- 26. Potter GB, Beaudoin GM 3rd, DeRenzo CL, et al. The hairless gene mutated in congenital hair loss disorders encodes a novel nuclear receptor corepressor. Genes Dev 2001 ; 15 : 2687-701.
- 27. Moraitis AN, Giguere V, Thompson CC. Novel mechanism of nuclear receptor corepressor interaction dictated by activation function 2 helix determinants. Mol Cell Biol 2002 ; 22 : 6831-41.
- 28. Moraitis AN, Giguere V. The co-repressor hairless protects RORalpha orphan nuclear receptor from proteasome-mediated degradation. J Biol Chem 2003 ; 278 : 52511-8.
- 29. Hsieh JC, Sisk JM, Jurutka PW, et al. Physical and functional interaction between the vitamin D receptor and hairless corepressor, two proteins required for hair cycling. J Biol Chem 2003 ; 278 : 38665-74.
- 30. Potter GB, Zarach JM, Sisk JM, Thompson CC. The thyroid hormone-regulated corepressor hairless associates with histone deacetylases in neonatal rat brain. Mol Endocrinol 2002 ; 16 : 2547-60.
- 31. Komuves LG, Michael E, Arbeit JM, et al. HOXB4 homeodomain protein is expressed in developing epidermis and skin disorders and modulates keratinocyte proliferation. Dev Dyn 2002 ; 224 : 58-68.
- 32. Braun KM, Niemann C, Jensen UB, et al. Manipulation of stem cell proliferation and lineage commitment : visualisation of label-retaining cells in wholemounts of mouse epidermis. Development 2003 ; 130 : 5241-55.
- 33. Taylor G, Lehrer MS, Jensen PJ, et al. Involvement of follicular stem cells in forming not only the follicle but also the epidermis. Cell 2000 ; 102 : 451-61.
- 34. Zarach JM, Beaudoin GM 3rd, Coulombe PA, Thompson CC. The co-repressor hairless has a role in epithelial cell differentiation in the skin. Development 2004 ; 131 : 4189-200.
- 35. Beaudoin GM 3rd, Sisk JM, Coulombe PA, Thompson CC. Hairless triggers reactivation of hair growth by promoting Wnt signaling. Proc Natl Acad Sci USA 2005 ; 102 : 14653-8.
List of figures
Figure 1
Le gène hairless chez la souris et les différentes mutations identifiées.
Figure 2
Phénotype des mutants hairless.
A. La première pousse de poils est d’apparence normale. B, C. Deux semaines après la naissance, les mutants développent une alopécie de l’avant vers l’arrière de leurs corps (B) qui aboutit à la perte totale et irréversible du pelage (C). D. Avec l’âge, la peau des animaux mutants a tendance à s’épaissir et à former des replis cutanés, particulièrement prononcés au niveau du museau.
Figure 3
Structure de la protéine Hairless.
Chez la souris, la protéine Hairless (HR) est composée de 1 182 acides aminés et présente une masse moléculaire de 127 kDa. Morphologiquement, la protéine Hairless ne possède pas de motifs structuraux distinctifs, à l’exception d’une séquence putative à doigt de zinc entre les acides aminés 590 et 625 (ZF). La protéine Hairless se localise dans le noyau, grâce à une séquence signal de localisation nucléaire bipartite (NLS, nuclear localisation signal), située entre les acides aminés 409 et 427. Des domaines d’interaction avec des récepteurs nucléaires d’hormones ont été identifiés dans la protéine Hairless de rat qui présente 95 % d'identité avec celle de la souris : les domaines d’interaction avec les récepteurs nucléaires de l’hormone thyroïdienne (TR) sont situés entre les acides aminés 750 et 864 (TR-ID1) et les acides aminés 980 et 1 084 (TR-ID2) ; la région située entre les acides aminés 750 et 864 comprend également le domaine d’interaction avec le récepteur de la vitamine D (VDR-ID), ainsi que les motifs LXXLL capables d’interagir avec le récepteur α-orphelin des rétinoïdes (RORα-ID). La protéine Hairless serait un corépresseur ; des analyses fonctionnelles ont révélé l’existence de trois domaines de répression, RD1, RD2, RD3, situés entre les acides aminés 236 et 450, 750 et 864, et 864 et 980, respectivement. La protéine HR est également capable de réguler la voie Wnt en réprimant le gène Wise, un inhibiteur de la voie Wnt.
Figure 4
Profil d’expression du transgène Hoxb4/LacZ au cours de l’embryogenèse.