Article body
C’est à la surface des lymphocytes T que l’antigène CD44 a été décrit pour la première fois [1]. Diverses appellations ont été attribuées à cette molécule, par référence tantôt à sa fonction tantôt à sa structure, soulignant ainsi l’impact de CD44 dans de nombreux processus physiologiques.
CD44 représente une famille de glycoprotéines transmembranaires de type I. La diversité de cette famille de protéines résulte, d’une part, de l’épissage alternatif des 10 exons, situés au centre du gène, désignés « variants » (pour revue, voir [2]). L’expression différentielle de ces variants explique l’importante diversité de la partie extracellulaire de la molécule (plus de 20 isoformes ont déjà été identifiées). De multiples modifications post-traductionnelles, correspondant principalement à des N- et O-glycosylations et à l’ajout de chondroïtine sulfate, contribuent aussi à la variabilité protéique au sein de cette famille (pour revue, voir [2]). La plus petite isoforme, dépourvue de variant, est appelée CD44 « standard » et est exprimée dans la plupart des tissus. En revanche, l’expression des isoformes comprenant des variants caractérise certains tissus à renouvellement rapide, comme la peau. En pathologie, en particulier dans les cancers, l’expression des variants est déterminante pour le développement de la maladie (pour revue, voir [2]).
Plus de 5000 articles consacrés à l’étude du CD44 ont été publiés depuis sa découverte. Dans un premier temps, c’est surtout le rôle de CD44 dans l’activation des lymphocytes (homing, migration, rolling) et la réponse immunitaire [3] qui a été étudié. La fonction de CD44 comme récepteur de l’acide hyaluronique, un composant crucial de la matrice extracellulaire, a également été très étudiée [4].
La découverte en 1991 de l’expression spécifique d’une nouvelle isoforme de CD44 contenant le variant v6 dans les cellules métastatiques de carcinome pancréatique de rat - et son absence dans les cellules non métastatiques correspondantes - a apporté un regain d’intérêt [5]. Des anticorps neutralisant l’activité de cette isoforme ont eu pour conséquence d’inhiber le pouvoir métastatique des cellules et, à l’inverse, l’introduction de cette isoforme dans des cellules non métastatiques leur a conféré la capacité de développer des métastases [5, 6]. Depuis cette découverte, de nombreuses études corrélatives ont révélé l’expression accentuée de certains variants de CD44 dans des tumeurs humaines, et dans certaines, comme le cancer du côlon, l’expression de certains variants est de mauvais pronostic. À l’inverse, le degré de malignité de certains cancers, comme les neuroblastomes ou encore le cancer de la prostate, est associé à la perte de CD44, suggérant que CD44 pourrait être un suppresseur de tumeur [2].
Malgré ces avancées, les mécanismes moléculaires par lesquels CD44 est impliqué dans le processus tumoral et métastatique n’étaient pas élucidés. Quelques publications récentes ont progressivement permis de réconcilier les observations apparemment contradictoires faisant de CD44 tantôt un promoteur, et tantôt un suppresseur de tumeur (Figure 1). Tout a commencé dans les années 1990 lorsqu’il s’est avéré que CD44 pouvait servir de molécule présentatrice de facteurs de croissance tels que MIP-1β [7]. Cette observation a ensuite été confirmée pour d’autres facteurs de croissance, comme le FGF (fibroblast growth factor) ou HB-EGF (heparin binding-epidermal growth factor), dont on connaissait la capacité de liaison à l’héparane sulfate et qui pouvaient également se lier aux isoformes de CD44 contenant l’exon v3 et modifiées par l’héparane sulfate [8]. La signification physiologique de cette interaction entre CD44 et des facteurs de croissance a été élucidée au cours de l’étude du développement des membres chez le rat. En effet, il a été démontré que les cellules épithéliales de l’AER (apical ectodermal ridge) expriment l’isoforme de CD44 contenant l’exon v3, modifiée par l’héparane sulfate [9]. CD44 séquestre alors le facteur de croissance FGF et le présente à son récepteur FGFR qui est exprimé par les cellules mésenchymateuses sous-jacentes. La prolifération de ces cellules est alors stimulée.
Figure 1
Schéma illustrant le rôle de CD44, promoteur ou inhibiteur de la croissance et de l´invasion cellulaires.
Pour promouvoir la croissance et l´invasion des cellules, CD44 s´associe aux récepteurs de facteurs de croissance et à leur ligands (ici c-Met et HGF). L´activation du récepteur n´est possible qu´au sein de ce complexe. La propagation du signal vers les cibles cytoplasmiques nécessite le cytosquelette et se fait par l´intermédiaire des protéines ERM. Dans le cas inverse où CD44 inhibe la croissance et l´invasion cellulaire, CD44 se lie à l´acide hyaluronique. Cela a pour conséquence l´activation du suppresseur de tumeur - la merline - qui est alors déphosphorylée. Sous cette forme, la merline se lie à CD44 à la place des protéines ERM et bloque la transduction du signal et par conséquent la prolifération des cellules. La merline est le produit du gène NF2. HGF: hepatocyte growth factor; c-Met: récepteur à activité tyrosine kinase; ERM: ezrin-radixin-moesin; →: activation; —|: inhibition.
Nous venons de démontrer qu’un mécanisme similaire intervenait dans le processus tumoral et métastatique [10]. Dans ce cas, CD44 interagit avec le récepteur à activé tyrosine kinase, c-Met, dont le ligand est le HGF (hepatocyte growth factor) appelé aussi SF (scatter factor) ((→) m/s 1999, n° 5, p. 645). c-Met et HGF/SF jouent un rôle décisif dans la migration des cellules musculaires au cours du développement de l’embryon et exercent de multiples fonctions dans l’induction de la prolifération, de la migration ou encore de la formation des tubules rénaux [11]. c-Met est souvent surexprimé ou muté dans de nombreux cancers, et notamment dans les cancers pancréatiques et coliques, tumeurs dont le développement fait intervenir CD44 (Figure 2). De plus, l’analyse du profil d’expression génique de cellules métastatiques et non métastatiques par la méthode SSH (suppressive subtractive hybridization) a confirmé que, dans les cellules de carcinome pancréatique de rat dans lesquelles CD44 agit comme un promoteur de tumeur, c-Met était surexprimé [12]. Nous avons apporté la preuve que l’interaction entre CD44 et c-Met permettait l’activation de c-Met. En effet, des anticorps dirigés contre CD44 bloquent cette activation [10]. La phosphorylation du récepteur ayant été rendue impossible, toutes les voies en aval de l’activation de c-Met ont été inhibées, parmi lesquelles la phosphorylation des cibles cytoplasmiques de c-Met, dont ERK. Il en résulte l’abolition des fonctions de c-Met, dont la dispersion des cellules ou scattering, ou encore leur migration à travers une matrice.
Figure 2
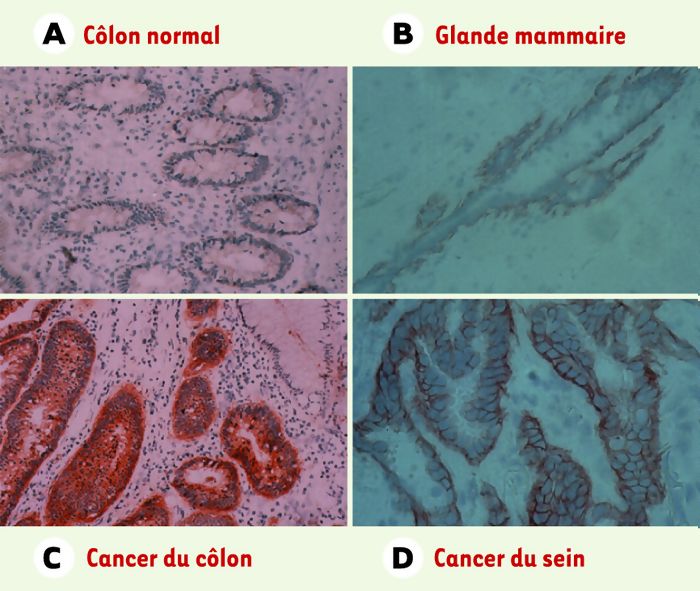
Expression tissulaire des isoformes de CD44 contenant l´exon v6.
A. Côlon sain. B. Glande mammaire. C. Polypes adénomateux du côlon. D. Tissu mammaire cancéreux. Le marquage a été réalisé avec un anticorps spécifique de CD44, v6, et avec de l´hématoxyline. On notera que, dans le tissu mammaire normal, seules les cellules myoépithéliales sont positives alors que, dans le tissu cancéreux correspondant, les cellules épithéliales sous-jacentes sont aussi marquées.
Comment expliquer cette intervention de CD44 dans l’activation de c-Met? Nous avons pu montrer que CD44 était nécessaire à la formation d’un complexe ternaire comprenant également HGF et c-Met. Ce n’est qu’au sein de ce complexe, que l’activation de c-Met est possible. Mais le rôle de CD44 ne s’arrête pas là. En effet, la partie cytoplasmique de CD44 est nécessaire à la transmission du signal du récepteur c-Met vers les cibles cytoplasmiques. En particulier, une courte séquence d’acides aminés basiques située à proximité de la membrane et qui permet l’attachement de molécules ERM (ezrin, radixin, moesin) -protéines reliant la membrane au cytosquelette - est décisive dans la propagation du signal [13].
Malgré toutes ces découvertes fascinantes, de nombreux aspects restent encore à explorer. La voie est maintenant ouverte pour d’autres découvertes. Comment se fait-il par exemple que l’activation de c-Met soit normale dans certaines cellules qui n’expriment pas CD44? Comment pouvons-nous expliquer le phénotype plus ou moins normal des souris dont le gène CD44 a été invalidé? Nous pensons que CD44 agirait comme co-récepteur de facteurs de croissance dans de nombreux cas - kératinocytes, lignées cellulaires établies, cellules cancéreuses - mais sans être un co-récepteur exclusif.
Comment expliquer le rôle de CD44 en tant que suppresseur de tumeur? Nous avons pu élucider ce mécanisme. En effet, le lien moléculaire et fonctionnel que nous avons mis en évidence concerne les molécules ERM. L’une des molécules appartenant à cette famille, la merline - produit du gène NF2 - est un suppresseur de tumeur [14]. Dans les conditions de culture où les cellules s’arrêtent de proliférer, la merline est active, déphosphorylée; elle se lie à CD44 et interfère avec les signaux de transduction, ce qui aboutit finalement à l’arrêt de la croissance cellulaire [15].
Les situations pathologiques dans lesquelles la fonction de CD44 en tant que co-récepteur de c-Met dominent donneraient lieu à une prolifération non contrôlée des cellules aboutissant au développement de tumeurs. Dans les quelques cas où les propriétés de CD44 en tant que suppresseur de tumeur dominent, l’inhibition de contact et l’arrêt de la croissance seraient alors promus par le couple CD44/merline.
Appendices
Références
- 1. Dalchau R, Kirkley J, Fabre JW. Monoclonal antibody to a human brain-granulocyte-T lymphocyte antigen probably homologous to the W 3/13 antigen of the rat. Eur J Immunol 1980; 10: 745-9.
- 2. Naor D, Sionov RV, Ish-Shalom D. CD44: Structure, function and association with the malignant process. In: Vande Woude GF, Klein G, eds. Advances in cancer research. San-Diego: Academic Press, 1997 : 243-318.
- 3. Haynes BF, Telen MJ, Hale LP, Denning SM. CD44: a molecule involved in leukocyte adherence and T-cell activation. Immunol Today 1989; 10: 423-8.
- 4. Sherman L, Sleeman J, Herrlich P, Ponta H. Hyaluronate receptors: key players in growth, differentiation, migration and tumor progression. Curr Opin Cell Biol 1994; 6: 726-33.
- 5. Günthert U, Hofmann M, Rudy S, et al. A new variant of glycoprotein CD44 confers metastatic potential to rat carcinoma cells. Cell 1991; 65: 13-24.
- 6. Seiter S, Arch R, Reber S, et al. Prevention of tumor metastasis formation by anti-variant CD44. J Exp Med 1993; 177: 443-55.
- 7. Tanaka Y, Adams DH, Hubscher S, Hirano H, Siebenlist U, Shaw S. T-cell adhesion induced by proteoglycan-immobilized cytokine MIP-1b. Nature 1993 : 361: 79-82.
- 8. Bennett KL, Jackson DG, Simon JC, et al. CD44 isoforms containing exon v3 are responsible for the presentation of heparin-binding growth factor. J Cell Biol 1995; 128: 687-98
- 9. Sherman L, Wainwright D, Ponta H, Herrlich P. A splice variant of CD44 expressed in the apical ectodermal ridge presents fibroblast growth factors to limb mesenchyme and is required for limb outgrowth. Genes Dev 1998; 12: 1058-71.
- 10. Orian-Rousseau V, Chen L, Sleeman JP, Herrlich P, Ponta H. CD44 is required for two consecutive steps in HGF/c-Met signaling. Genes Dev 2002; 16: 3074-86.
- 11. Birchmeier C, Gherardi E. Developmental roles of HGF/SF and its receptor, the c-Met tyrosine kinase. Trends Cell Biol 1998; 8: 404-10.
- 12. Nestl A, Von Stein OD, Zatloukal K, et al. Gene expression patterns associated with the metastatic phenotype in rodent and human tumors. Cancer Res 2001; 61: 1569-77.
- 13. Legg JW, Isacke CM. Identification and functional analysis of the ezrin-binding site in the hyaluronan receptor, CD44. Curr Biol 1998; 8: 705-8.
- 14. Rouleau GA, Merel P, Lutchman M, et al. Alteration in a new gene encoding a putative membrane-organizing protein causes neuro-fibromatosis type 2. Nature 1993; 363: 515-21.
- 15. Morrison H, Sherman LS, Legg J, et al. The NF2 tumor suppressor gene product, merlin, mediates contact inhibition of growth through interactions with CD44. Genes Dev 2001; 15: 968-80.
List of figures
Figure 1
Schéma illustrant le rôle de CD44, promoteur ou inhibiteur de la croissance et de l´invasion cellulaires.
Pour promouvoir la croissance et l´invasion des cellules, CD44 s´associe aux récepteurs de facteurs de croissance et à leur ligands (ici c-Met et HGF). L´activation du récepteur n´est possible qu´au sein de ce complexe. La propagation du signal vers les cibles cytoplasmiques nécessite le cytosquelette et se fait par l´intermédiaire des protéines ERM. Dans le cas inverse où CD44 inhibe la croissance et l´invasion cellulaire, CD44 se lie à l´acide hyaluronique. Cela a pour conséquence l´activation du suppresseur de tumeur - la merline - qui est alors déphosphorylée. Sous cette forme, la merline se lie à CD44 à la place des protéines ERM et bloque la transduction du signal et par conséquent la prolifération des cellules. La merline est le produit du gène NF2. HGF: hepatocyte growth factor; c-Met: récepteur à activité tyrosine kinase; ERM: ezrin-radixin-moesin; →: activation; —|: inhibition.
Figure 2
Expression tissulaire des isoformes de CD44 contenant l´exon v6.
A. Côlon sain. B. Glande mammaire. C. Polypes adénomateux du côlon. D. Tissu mammaire cancéreux. Le marquage a été réalisé avec un anticorps spécifique de CD44, v6, et avec de l´hématoxyline. On notera que, dans le tissu mammaire normal, seules les cellules myoépithéliales sont positives alors que, dans le tissu cancéreux correspondant, les cellules épithéliales sous-jacentes sont aussi marquées.